Любой гормональный сбой это провоцирующий фактор для развития многих серьезных заболеваний и симптомов.
Андростендион — гормон группы андрогенов, который выполняет важные эндокринные функции в организме женщины.
Его повышение в сыворотке крови нельзя оставлять без внимания. Это может привести к гинекологическим или другим аутоиммунным патологиям.
Не занимайтесь самолечением! Обязательно проконсультируйтесь с квалифицированным врачом. Информация носит ознакомительный характер и не заменяет медицинскую помощь.
За что отвечает
Андростендион — это андрогенный гормон, который обеспечивает полноценную выработку тестостерона и эстрогена.
Считается, что андрогены — это мужские гормоны, но у женщин они тоже есть.
В женском организме их концентрация намного меньше, чем у мужчин, но они также необходимы для репродуктивной системы.
Образование андростендиона — необходимый этап синтеза таких важных гормонов, как тестостерон и эстроген.
Эстрогенами называют определенную группу гормонов, которые формируют женскую репродуктивную систему. Тестостерон, наоборот, свойственен мужскому полу.
С биологической точки зрения андростендион просто предшествует их конечному образованию. Здесь есть прямая связь, так как неправильная выработка гормонов нарушает функционирование всей сексуальной и репродуктивной систем.
У женщин это может вызвать серьезные заболевания вплоть до онкологии.
Первоначальная секреция происходит в надпочечниках и яичниках. Работа этих органов косвенно зависит от андростендиона, стимулирующего их активность.
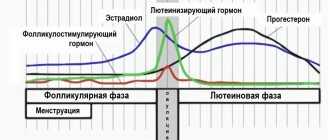
Его уровень постоянно изменяется в зависимости от возраста, времени суток, менструального цикла. Но значительное повышение гормона (гиперандрогения) в сыворотке крови требует врачебного вмешательства.
Все это предшествует ярко выраженной симптоматике, которая заставляет пациентов обратиться за помощью.
Уровень андростендиона проверяют путем лабораторного анализа венозной крови методом иммуноанализа (ИФА). Это исследование требует предварительной подготовки:
- Сдача биоматериала происходит в первые 3 дня менструального цикла.
- Усиленные физические тренировки и нагрузки должны быть исключены за неделю до взятия крови.
- От алкоголя и курения нужно воздержаться за 3 дня до исследования.
- Перед анализом нельзя употреблять пищу на протяжении 8-11 часов.
Это несложные правила, которые должны быть соблюдены для достоверности результатов.
Сейчас не существует другой альтернативы исследования, потому что анализ достаточно точно выявляет и подсчитывает уровень андростендиона.
Кровь можно сдать в государственной поликлинике бесплатно или в частной лаборатории за деньги. Полученные результаты понадобятся для дальнейших диагностических мероприятий.
Для чего необходимо сдать анализ на гормоны при планировании беременности?
О том, каковы признаки гормонального сбоя у женщин, расскажет наша публикация.
О гормональном сбое после медикаментозного прерывания беременности и его причинах читайте здесь в статье.
Причины гиперандрогении
Выделяют три основных типа генеза этого заболевания:
- Яичникового;
- Надпочечникового;
- Смешанного.
Женская гиперандрогения может возникнуть из-за неправильной работы гипоталамо-гипофизарной системы, к которой относится повышение и снижение уровня различных гормонов. Помимо этого выделяют наследственную и приобретенную формы болезни.
Также существует абсолютная и относительная формы гиперандрогении у женщин. Первый тип характеризуется появлением большого количества андрогенов — мужских стероидных половых гормонов. Вторая — с оптимальным количеством этих веществ, которые обладают усиленным метаболизмом.
Абсолютная гиперандрогения является следствием синдрома поликистозных яичников. Если в женском теле содержится большое количество пролактина, то процесс образования андрогенов увеличивается.
Причиной транспортного типа гиперандрогении может служить недостаток глобулина, отвечающего за иммунные свойства организма и свертываемости крови.
Причины увеличения показателей
Показатели андростендиона меняются согласно возрастным критериям, полу, дню менструального цикла. Очень сложно утвердить единую норму этого показателя.
При расшифровке результатов крови необходимо смотреть на референсные значения лаборатории. Они станут основополагающими в диагностике.
У детей, начиная с семилетнего возраста, стремительно повышается концентрация андростендиона. У людей в возрасте 30 лет и старше резко снижается.
По физиологическим причинам его высокий уровень выявляется в середине менструального цикла, а потом его значения идут на спад. Нарушение правил подготовки к анализу приводит к искажению результату в виде увеличения гормона.
В лабораториях рассматривают показатели в диапазоне от 3 до 10 нмоль/л или от 0,3-3,4 нг/мл. Все зависит от единицы измерения и методики исследования.
Увеличение цифр андростендиона — серьёзный признак патологии, поэтому требуется обследование.
Чаще его повышение может произойти в результате следующих заболеваний и состояний:
- поликистоз яичников;
- андрогенпродуцирующие (АКТГ) опухоли органов малого таза, надпочечников;
- синдром Иценко-Кушинга (гиперкортицизм);
- гипертекоз яичников (патологическое двустороннее увеличение);
- гиперплазия коры надпочечников (врожденное заболевание);
- нарушение функции щитовидной железы;
- остеопороз.
Врачу нужно выявить причины гиперандрогении, так как вызвать такую патологию могут многие заболевания.
Жалобы пациента и дополнительные анализы смогут прояснить клиническую картину. Правильная диагностика — это первая стадия лечения.
Причины пониженного андростендиона
В недостаточном количестве гормон вырабатывается в следующих случаях:
- Надпочечниковая недостаточность. Кора надпочечников теряет способность вырабатывать гормоны в нужном количестве, что приводит к нарушению обмена веществ.
- Истощение яичников. Как следствие, наступает ранний климакс. Могут пострадать нервная, репродуктивная и другие системы.
- Серповидноклеточная анемия. Главная особенность патологии заключается в том, что меняется форма эритроцитов.
Иногда гормон андростендион вырабатывается в недостаточном количестве после длительного применения гормональных контрацептивов. Перед приемом гормональных препаратов для контрацепции обязательно нужно проконсультироваться с врачом и пройти обследование. Специалист подберет препарат и рассчитает правильную дозировку.
Определение содержания андростендиона в крови может потребоваться при диагностике заболеваний репродуктивной системы и надпочечников. Назначить анализ может гинеколог или эндокринолог. Проводят исследование в следующих случаях:
- бесплодие;
- серьезные нарушения менструального цикла (длительные задержки, нерегулярность) или его отсутствие;
- ранее половое созревание;
- задержки в половом созревании;
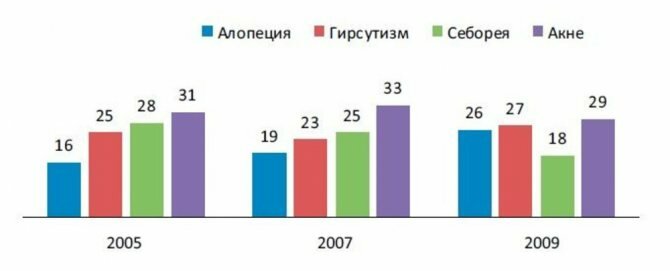
- облысение;
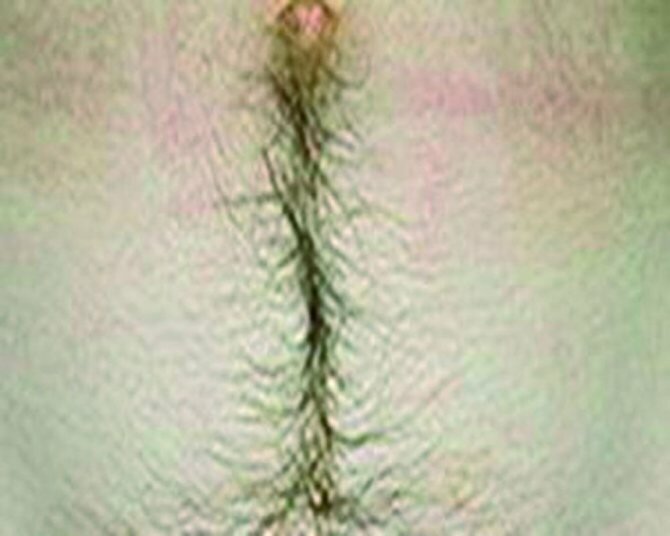
- гирсутизм (появление волос по мужскому типу – на лице, на животе и др.);
- маточные кровотечения, не связанные с менструальным циклом;
- появление угревой сыпи после полового созревания.
Проводиться исследование может и при опухоли яичников или надпочечников. Решение о необходимости выполнения анализа принимает врач. Дополнительно проводятся другие клинические исследования. Они помогают поставить правильный диагноз.
Высокий уровень во время беременности и после родов
В период беременности у женщины повышаются в основном все гормоны, потому что плод начинает стремительно развиваться. Это нормальное состояние, не требующее корректировки.
Андростендион тоже немного повышается, начиная с 1 недели беременности.
Сильное повышение гормона чревато выкидышем, различными патологиями плода. Это особенно опасно в первый триместр беременности, а в остальных случаях паниковать не нужно.
После родов гиперандрогения обычно исчезает, все приходит в норму. При повышенных значениях гормона практически невозможно зачать ребенка, поэтому беременность при гиперандрогении маловероятна.
Многие врачи не видят смысла заниматься тщательным эндокринным мониторингом во время беременности, так как гормональный дисбаланс проявляется на физиологическом уровне.
Лучше заниматься диагностикой уже после беременности. Однако, некоторые врачи начинают выписывать гормональные таблетки (Дексаметазон), чтобы понизить гормон.
Такое лечение проводится в случае острой необходимости, когда плоду угрожает опасность из-за сильного повышения андростендиона.
Во время беременности нельзя принимать гормональные средства. Такие препараты имеют серьезные побочные эффекты, а развитие плода уже в зоне риска.
Пониженный андростендион у женщин
Гормон андростендион редко в организме женщины вырабатывается в недостаточном количестве, хотя подобное явление не менее опасное, чем чрезмерный его синтез. Если отклонения от нормы большие, вероятность развития бесплодия довольно высокая. При нехватке гормона зачать ребенка практически невозможно.
Основные симптомы пониженного андростендиона:
- снижение либидо;
- гиперпигментация кожных покровов;
- нарушение менструального цикла;
- уменьшение яичников в размерах (хотя в некоторых случаях происходит их увеличение);
- снижение артериального давления.
Пониженный андростендион обнаруживается при обследовании, когда женщина обращается к врачу из-за невозможности забеременеть. На иные симптомы пациентка обычно не обращает внимания или связывает их с другими патологиями.
Симптомы и признаки
Обычно женщина наблюдает у тебя яркую симптоматику, которая предшествует обращению к врачу. Андростендион по своему действию намного слабее тестостерона. Но его высокая концентрация может вызывать внешние изменения у женщины по типу маскулинизации.
У гиперандрогении много симптомов, которые могут по-разному проявляться. Это зависит от общего гормонального фона и организма.
Симптоматика гиперандрогении:
- Нарушение менструального цикла (прекращение, задержка).
- Кровотечения в середине цикла.
- Вирилизация (изменение тембра голоса, чрезмерная волосяная растительность на теле и лице).
- Угревая сыпь на лице, не поддающаяся лечению (акне).
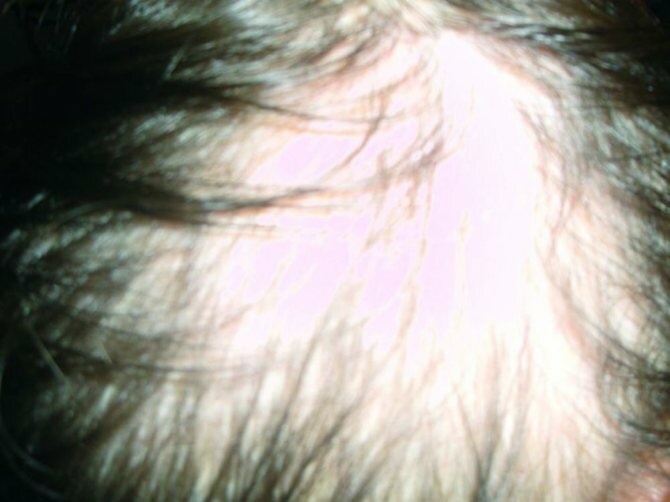
- Облысение затылочной части головы (алопеция).
- Жировые отложения в животе.
- Увеличение веса, происходящее за счет роста мышц и жира.
- Раннее развитие половых органов.
- Выкидыш.
- Бесплодие.
Все эти состояния требуют врачебного наблюдения и помощи. Нельзя медлить или дожидаться новых симптомов, так как гормональный фон нужно корректировать.
При незначительной гиперандрогении симптомов может не быть или они будут проявляться совсем незначительно. Но чаще это следствие физиологических причин (фаза менструального цикла, приём лекарств, первый триместр беременности). При серьезной патологии всегда заметны клинические признаки.
О том, какие гормональные таблетки при миоме матки может назначить доктор, читайте на текущей странице.
О гормональном бесплодии у женщин расскажет наша публикация.
Какие гормональные препараты при климаксе могут понадобиться, читайте в этом материале.
Норма андростендиона у женщин
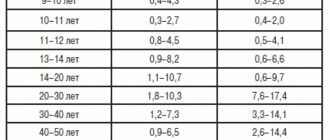
Главная особенность гормона заключается в том, что его концентрация постоянно изменяется. Показатели уровня андростендиона колеблются в определенных рамках на протяжении всей жизни. У детей он практически отсутствует. В больших количествах гормон начинается вырабатываться с 9-10 лет и увеличивается в подростковом возрасте. Высокая концентрация удерживается до 30 лет, а потом выработка снижается.
Норма андростендиона у женщин детородного возраста составляет 1,6 — 19 нмоль/л.
Уровень гормона может меняться в зависимости от фазы менструального цикла. На выработку гормона влияет питание, физическая активность и другие факторы, концентрация гормона обычно меняется и в течение дня.
Опасно ли состояние
Длительно протекающая гиперандрогения провоцирует развитие заболеваний и осложнений. Нельзя надеяться, что гормональный фон восстановится сам без врачебной помощи.
У женщины постепенно начинается вирилизация, то есть маскулинизация, обретение мужских черт. Голос становится более низким и грубоватым, а волосы начинают расти по всему телу, тип фигуры становится мужским.
Такое состояние может усугубляться без должного лечения. У женщины наблюдаются гинекологические заболевания и симптомы (отсутствие менструации, поликистоз или гиперплазия яичников).
Однако, последствия этими осложнениями не ограничиваются. Опасность гиперандрогении в следующих возможных патологиях:
- Аутоиммунное заболевание Иценко-Кушинга, которое очень плохо поддается лечению.
- Сильное ожирение.
- Опухоли яичников, продуцирующие гормон АКТГ.
- Злокачественные новообразования органов малого таза.
- Сахарный диабет 2 типа.
- Остеопороз.
- Мышечная дистрофия.
- Облысение.
Самое опасное — онкология, так как опухоли, продуцирующие гормон АКТГ, в 30% случаев перерождаются в злокачественные новообразования. Поэтому нужно своевременно начинать корректирующую гормонотерапию.
Гиперандрогения надпочечной природы обычно проявляется с рождения. У женщины рано проявляются мужские половые признаки и тип фигуры. Это тоже требует лечения, так как возможны аналогичные последствия.
К какому врачу нужно обратиться, диагностика
Гормональные отклонения требуют острожного и индивидуального подхода. Обычно такими проблемами занимаются следующие специалисты:
- эндокринолог;
- гинеколог-эндокринолог;
- гинеколог.
Пациент может обратиться к любому, так как все они обладают достаточной компетенцией в подобных вопросах.
Гинеколог-эндокринолог имеет узкую специализацию в лечении гормональных патологий репродуктивной системы женщин. Но такой доктор есть далеко не во всех клиниках.
Эндокринолог занимается общими эндокринными патологиями у обоих полов, но чаще гиперандрогенией занимается гинеколог.
К таким специалистам можно обратиться бесплатно как в государственных поликлиниках, так и в частных медицинских центрах за деньги.
Врач, посмотрев на результаты анализов, назначит дополнительное обследование и диагностику, чтобы точно понять, насколько серьезна патология.
Это потребует времени и терпения, потому что нужно назначить эффективное лечение. Чаще врач назначает следующие диагностические процедуры:
- Анализ крови на другие гормоны (прогестерон, тестостерон, эстрадиол, пролактин, кортизол, лютеинизирующий гормон, ФСГ, ДЭА, ТТГ, АКТГ, альдостерон).
- УЗИ-исследование органов малого таза, щитовидной железы и почек.
- Кольпоскопия.
- КТ-диагностика с контрастом органов малого таза.
- МРТ, рентгенография почек и надпочечников.
На основе полученных результатов врач назначает развернутое лечение. Необходимо сделать полный гормональный скрининг. Это позволит определить общее состояние пациента.
УЗИ, КТ, МРТ — дополнительные методы обследования. Они необходимы, чтобы исключить опухоли, новообразования, рассчитать размеры надпочечников и яичников (гиперплазия).
Лечение
Гиперандрогения успешно поддается лечению. Но начинать терапию нужно на первоначальном этапе или с самого раннего возраста, если заболевание имеет врожденный характер (надпочечная гиперплазия).
В качестве коррекции уровня андростендиона используется гормональная терапия. Она подбирается строго индивидуально после проведенного обследования.
Сейчас используются такие категории препаратов для восстановления эндокринного дисбаланса:
- Оральные контрацептивы.
- Глюкокортикостероиды.
- Эстрогенные лекарства.
- Антиандрогенные препараты.
- Диетотерапия.
- Косметологические процедуры (удаление волос различными методиками).
- Коагуляция (прижигание) яичников.
- Хирургическое вмешательство при наличии опухолей.
Оральные контрацептивы эффективны при лечении болезни, так как они содержат комбинацию женских гормонов (эстроген и прогестин).
Врачи часто назначают препарат Диане-35. Лекарство обладает антиандрогенным свойством, то есть используется для устранения роста волос на теле и лице (гирсутизм).
В качестве альтернативы врачи выписывают другие контрацептивы: Марвелон, Овидон, Фемоден. Их необходимо принимать длительно (около 1 года), чтобы достигнуть терапевтических результатов. Но такие препараты имеют серьезные побочные эффекты.
Женщины с сердечно-сосудистой патологией и диабетом 2 типа не могут их принимать. Поэтому врачами назначаются глюкокортикостероиды. Они также используются при тяжелых формах заболевания.
Популярными глюкокортикостероидами считаются таблетки Дексаметазон, Мегадексан, Метипред, Преднизолон, которые выписывают в минимальной дозировке.
Из эстрогенных лекарств успешно себя зарекомендовал Кломифен. Он восстанавливает менструальный цикл, используется при лечении бесплодия.
Цитопротерон — популярное антиандрогенное средство. Оно подавляет действие андростендиона, устраняя симптоматику маскулинизации.
Врач при назначении лечения использует комбинированную терапию, сочетая разные препараты. Он определяет дозировку и длительность приёма.
Хирургическое вмешательство используется только при наличии опухолей яичников и надпочечников.
Вы знаете, каковы причины и симптомы того, что повышен гормон пролактин у женщин? Ответ на вопрос ищите в этой публикации. Каковы симптомы нехватки гормонов щитовидной железы у женщин? Об этом расскажет наша статья.
Гиперандрогения — состояние, связанное с избыточной секрецией андрогенов и/или их усиленным воздействием на организм, которое у женщин чаще всего проявляется вирилизацией (появление мужских черт).
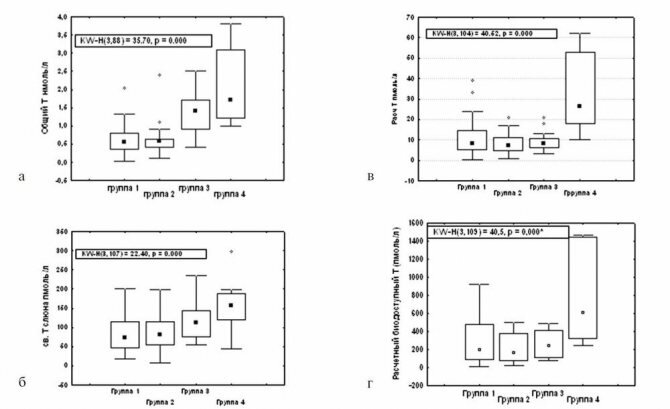
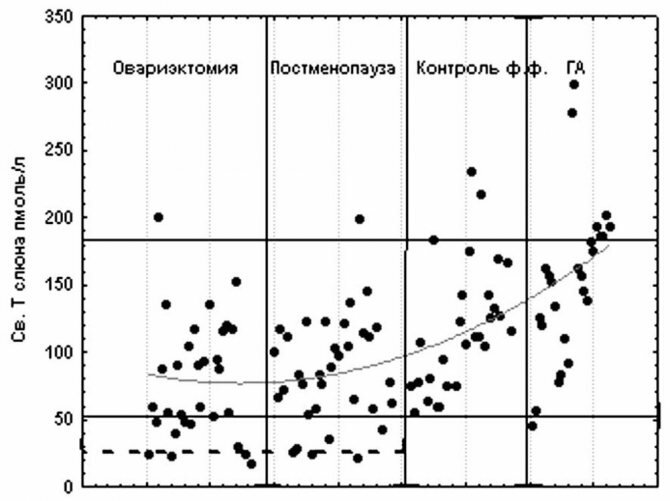
У женщин циркулирующие в крови андрогены (группа стероидных гормонов) в норме синтезируются в яичниках и надпочечниках, а также путем периферической конверсии андростендиона (АНД) и дегидроэпиандростерона (ДГЭА) в тестостерон (Т). В клинической практике большое значение имеют следующие андрогены и их предшественники: тестостерон, дигидротестостерон (ДГТ), 17-ОН-прогестерон (17-оксипрогестерон), АНД, дегидроэпиандростерон-сульфат (ДГЭАС).
Среди всех эндокринных заболеваний в гинекологической практике чаще всего встречаются патология щитовидной железы и рассматриваемая нами гиперандрогения. Для понимания данной проблемы необходимо обратиться к схеме синтеза андрогенов, как можно более упростив ее. Весь процесс в основном контролируется гормонами гипофиза — АКТГ (аденокортикотропным гормоном) и ЛГ (лютеинизирующим гормоном). Синтез всех стероидных гормонов начинается с превращения холестерина в прегненолон. Важно понимать следующее: этот этап происходит во всех стероидпродуцирующих тканях! Остальные процессы также в той или иной степени происходят во всех органах, имеющих отношение к стероидогенезу, однако в результате разными органами продуцируются как одинаковые, так и разные стероидные гормоны.
Кроме того, необходимо добавить, что продукция стероидных гормонов может происходить не только в эндокринных органах, но также и на периферии. В частности, для женщины важную роль в продукции стероидов играет подкожная жировая клетчатка.
Большинство врачей не считают необходимой оценку уровней андрогенов у женщин в постменопаузе при наличии клинических симптомов или биохимически подтвержденного их повышения из-за отсутствия взаимосвязи их уровней с различными изменениями в организме, возникающими в период естественного процесса старения. Однако при наличии клинических симптомов гиперандрогении следует обязательно проводить дифференциальную диагностику заболеваний, которые приводят к избытку андрогенов у женщин в постменопаузе. Рассмотрение возможных ключевых моментов в анамнезе, при физикальном обследовании и соответствующей лабораторной и рентгенологической оценке приведет к подбору оптимальных стратегий лечения выявленных причин гиперандрогении.
Ведущие признаки и симптомы
Большинство женщин с гиперандрогенией в период постменопаузы жалуются на гирсутизм в области лица и/или туловища вместе с потерей волос на голове. Подробный анамнез имеет решающее значение в разграничении прогрессирующего гирсутизма от истинной вирилизации. Гирсутизм — это избыточный рост терминальных волос, особенно на подбородке, верхней губе и в области белой линии живота [13]. Степень гирсутизма можно оценить по шкале Ферримана-Галлвея (1961), которая описывает степень роста волос в баллах от 0 до 4 в 9 областях тела. Считается, что у женщин в период пременопаузы степень гирсутизма равна 8 баллам и более, хотя в постменопаузе общий балл не обладает такой достоверностью. Вирилизация — комбинация выраженного гирсутизма вместе с облысением по мужскому типу, анаболическим (андроидным) типом ожирения, снижением тембра голоса и клиторомегалией (≥1,5×2,5 см) [13]. Наличие симптомов вирилизации предполагает выраженную гиперандрогению и необходимость проведения обследования для обнаружения опухоли (см. таблицу).

Синдром поликистозных яичников (СПКЯ)
СПКЯ (синдром Штейна-Левенталя) — сочетание олигоменореи или аменореи и двусторонних множественных кист яичников. При этом заболевании чаще всего встречаются нарушение менструального цикла, бесплодие, гирсутизм и ожирение [4]. Диагноз ставится при наличии гиперандрогении и хронической ановуляции [2]. При СПКЯ повышен риск развития инсулинорезистентности и гиперинсулинемии; сахарный диабет наблюдается у 20% больных.
Женщины с СПКЯ составляют особую группу, так как данное заболевание сохраняется вплоть до периода менопаузального перехода. В виду того что синтез Т яичниками снижается при естественной менопаузе постепенно [6], симптомы гиперандрогении, связанные с СПКЯ, могут сохраняться. Тщательно собранный анамнез, подтверждающий регулярность менструального цикла, время проявления симптомов гиперандрогении и прибавки массы тела помогут определить точный диагноз [20]. Поскольку женщины с СПКЯ имеют повышенный риск развития метаболического синдрома, сахарного диабета 2-го типа и гиперпластических процессов в эндометрии [15], должны быть определены методы раннего их выявления и проведено соответствующее лечение.
Гиперандрогения, вызванная ожирением
Известно, что не все женщины с избыточной массой тела имеют СПКЯ. В клинической практике широко распространено сочетание ожирения и симптомов, схожих с СПКЯ, но они сильно отличаются от симптомов классического СПКЯ, в связи с чем была выделена отдельная группа женщин с «гиперандрогенией, вызванной ожирением» [19]. Для таких женщин обычно характерно своевременное наступление менархе и регулярный менструальный цикл, но часто есть связь прибавки массы тела в анамнезе с беременностью без ее снижения до исходного уровня в течение последующих лет. На этом фоне менструальный цикл у женщин с наступлением периода пременопаузы становится нерегулярным. Позже развиваются признаки гиперандрогении, часто с образованием кист в яичниках, но без повышенного соотношения ЛГ/ФСГ, характерного для СПКЯ. Предполагают, что избыток ароматазы и 5α-редуктазы в жировой ткани вызывает местное повышение уровня эстрогенов и андрогенов, что приводит к нерегулярному циклу, гирсутизму и акне соответственно. Схожий сценарий наблюдается при достижении критической пороговой массы тела в период постменопаузы. В этом случае анамнез и время прибавки массы тела также помогут разграничить гиперандрогению при СПКЯ или вызванную ожирением. Стигмы, характерные для СПКЯ, помогают поставить диагноз, но они не исчезают при снижении массы тела. Как показывает клиническая практика, фенотипические симптомы гиперандрогении, вызванные ожирением, при снижении массы тела исчезают.
Дифференциальная диагностика СПКЯ и гиперандрогении, вызванной ожирением, у женщин в постменопаузе достаточно сложна. В то время как уровни Т резко падают при хирургической менопаузе, естественная менопауза приводит к более постепенному снижению уровня Т с возрастом (H. Judd и соавт., 1974). S. Winters и соавт. [26] доказали, что уровни Т всегда выше у женщин с СПКЯ по сравнению с женщинами контрольных групп соответствующего возраста. Однако недостатком данного исследования является то, что самая старшая возрастная группа включала женщин только от 47 до 57 лет и не была разделена по статусу относительно возраста наступления менопаузы. Не было также данных по изучению детального изменения уровней андрогенов у женщин с СПКЯ после менопаузы по сравнению с такими данными у женщин с ожирением с таким же индексом массы тела (ИМТ), не имевших СПКЯ.
Синдром Кушинга
Синдром Кушинга — состояние, характеризующееся избытком продукции глюкокортикоидов надпочечниками. У большинства больных отмечается увеличение массы тела с отложением жира на лице (лунообразное лицо), шее, туловище. Характерными клиническими проявлениями являются гирсутизм, нарушение менструальной функции, бесплодие, атрофия мышц конечностей, остеопороз, снижение иммунорезистентности, нарушение толерантности к глюкозе, депрессия и психозы. Существуют следующие варианты синдрома:
А. АКТГ-зависимый синдром гипофизарный — чаще всего опухолевое поражение гипофиза — и эктопический — секреция АКТГ (или кортиколиберина) опухолью любой локализации.
Б. АКТГ-независимый синдром надпочечниковый — рак, аденома или гиперплазия коры надпочечников — и экзогенный — самолечение препаратами глюкокортикоидов или вынужденный прием данных препаратов при другой патологии.
Гипертекоз (синдром Френкеля)
Гипертекоз яичников — двустороннее разрастание стромы яичников за счет пролиферации и лютеинизации. Клинически проявляется высокой вирилизацией женского организма вследствие выработки стромальными клетками яичника ДГЭА, андростендиона и Т. В плазме значительно повышено содержание эстрона (Э1). Соотношение ЛГ и ФСГ в норме или снижено. Кломифеновая проба отрицательная.
Еще в 1942 г. J. Gains отметил связь между клиническими проявлениями вирилизации и наличием островков лютеинизированных клеток в строме яичников. Впоследствии это явление стали называть стромальным гипертекозом. По мнению Е.Г. Иванова, гипертекоз — это наличие группы лютеинизированных клеток, которые расположены участками или диффузно в строме, захватывают область химуса. В отличие от СПКЯ, при гипертекозе кистозно атрезирующиеся фолликулы имеются в небольшом количестве либо отсутствуют, а белочная оболочка чаще всего не утолщена.
Гипертекоз является тяжелой формой СПКЯ, приводит к чрезмерной продукции андрогенов стромальными клетками яичников (S. Braithwaite и соавт., 1978). Это заболевание может проявиться у женщин как в пре-, так и в постменопаузе. Хотя основная этиология заболевания неясна, но считается, что причина гипертекоза яичников связана с повышенным уровнем гонадотропинов, в основном, ЛГ [12]. Яичники могут иметь нормальные размеры для пременопаузы, но не для постменопаузы; поэтому при интерпретации результатов УЗИ необходимо учитывать возраст женщины и период климактерия [3]. При гипертекозе наряду с гиперсекрецией андрогенов также повышена продукция эстрогенов на периферии, и эти женщины часто относятся к группе риска развития гиперплазии эндометрия и карциномы яичников [12]. Наличие симптомов СПКЯ в анамнезе может помочь при проведении дифференциальной диагностики. Женщины с гипертекозом имеют риск развития метаболических осложнений — гиперлипидемии и сахарного диабета 2-го типа [12, 16], хотя крупных исследований, в которых бы изучались их частота, клинические проявления и отдаленные последствия у таких пациенток в постменораузе, не проводилось.
Таким образом, гипертекоз — это неопухолевая патология яичников, при которой в их строме появляются пролиферирующие островки лютеинизированных клеток. При гипертекозе продукция Т, АНТ и ДГЭА возрастает в большей степени, чем при СПКЯ. Уровни ЛГ и ФСГ могут быть нормальными или сниженными, а степень инсулинорезистентности и гиперинсулинемии превышает таковую при СПКЯ.
Опухоли яичников или надпочечников
У женщин с опухолями яичников или надпочечников имеются быстро прогрессирующие признаки вирилизации, обусловленные высоким уровнем андрогенов.
Андробластома — односторонняя опухоль яичника, встречается в любом возрасте. Оказывает на организм женщины двухфазное воздействие: дефеминизацию, а затем маскулинизацию. Характерна гипоменорея, затем аменорея, выраженный гирсутизм, гипертрофия клитора, гипоплазия матки и молочных желез; в менопаузе — облысение, изменение тембра голоса.
Гистологическая картина ткани опухолей яичников у больных с гиперандрогенией представлена опухолевыми клетками Лейдига, Сертоли и стероидными клетками яичника (L. Morgan, 1990). Число случаев этих опухолей составляет 10% среди всех опухолей яичников. В источниках литературы описаны менее 150 случаев опухолей, состоящих только из опухолевых клеток Лейдига [11]. Данный тип опухоли продуцирует T и/или другие фракции андрогенов наряду с эстрогенами или без последних.
Опухоли надпочечников секретируют прогормоны андрогенов: ДГЭА, ДГЭАС и реже T, глюкокортикоиды и/или эстрогены [14, 23]. Истинную болезнь Кушинга следует дифференцировать от негипофизарного синдрома Кушинга, при котором избыточность эндогенного кортизола служит проявлением так называемого эктопического или паранеопластического АКТГ-синдрома (АКТГ-зависимый избыток глюкокортикоидов), аденомы или карциномы коры надпочечников или же экзогенного поступления глюкокортикоидов (АКТГ-независимый избыток глюкокортикоидов). При гормональном обследовании у больных с синдромом Кушинга определяются очень высокий уровень кортизола (гиперкортизолизм), высокий уровень T, но, как правило, несколько сниженный уровень ДГЭАС [28]. В противоположность этому при карциноме надпочечников наблюдаются высокие уровни ДГЭАС, хотя опухоль растет медленно и диагностируется при размерах больше 8-10 см. Однако описаны случаи опухолей надпочечников, секретирующих не только ДГЭАС, но и T [5].
Врожденная гиперплазия коры надпочечников
Врожденная гиперплазия коры надпочечников (ВГКН) — наследственное генетическое заболевание, связанное с наследственным дефицитом 11β- или 21-гидроксилазы.
В зависимости от этнической принадлежности пациентки различают 2 формы ВГКН: врожденная гиперплазия коры надпочечников, классическая (редко) или неклассическая (чаще), может быть причиной гиперандрогении в постменопаузе [22]. Семейный анамнез раннего пубархе, низкорослость и этническая принадлежность (повышенный риск у эскимосов, ашкенази, испанцев, итальянцев) позволяют предположить ВГКН, для подтверждения которой необходимо проведение лабораторной и инструментальной оценки. При этом повышается синтез кортикостероидов, что приводит к стимуляции выделения гипофизом АКТГ, а это в свою очередь ведет к усиленной секреции андрогенов корой надпочечников с последующей ее гиперплазией. Наряду с вирилизацией у больных развиваются слабость, мышечные боли, снижение артериального давления, пигментация кожных покровов. Уровень 17-ОКС в моче снижен, но при увеличении общего уровня 17-КС увеличивается уровень ДГЭА. Рентгенологически тень надпочечников более интенсивна при гиперплазии, чем при опухоли.
Лечение [19] ингибиторами ароматазы при раке молочной железы может спровоцировать гиперандрогению у женщин в постменопаузе с ранее неизвестной ВГКН.
Ятрогенная гиперандрогения
Применение лекарственных препаратов и/или пищевых добавок, а также гель с Т, используемый партнером, может привести к гирсутизму у женщин в постменопаузе [13]. Для лечения менопаузальных симптомов некоторые женщины используют комбинацию эстрогенов с Т или ДГЭА, которые в фармакологических дозах вызывают гирсутизм и другие симптомы гиперандрогении. Тщательный анализ лекарственных препаратов, пищевых добавок и гормональной терапии партнера поможет выявить эти обратимые причины.
Лабораторные исследования
Изучение анамнеза и физикальный осмотр проводят перед лабораторным и инструментальным исследованиями. Наиболее важным лабораторным исследованием для выявления гиперандрогении является определение уровней тестостерона и ДГЭАС [13]. Определение ДГЭА малоинформативно, так как этот гормон имеет неустойчивый ритм в течение суток и меняется при стрессе. Большинство коммерческих тестов были разработаны для определения общего Т у мужчин, поскольку порог чувствительности уровня Т у женщин очень низкий [17]; тем не менее уровни Т, значительно превышающие пределы нормального диапазона, могут быть использованы для диагностики гиперандрогении и контроля за ее динамикой во время лечения [17, 22]. Учитывая, что секреция андрогенов в яичниках и надпочечниках снижается с возрастом [6], следует критически относиться к достоверности оценки уровня андрогенов при гиперандрогении в пожилом возрасте. Относительно недавно разработаны тест-системы для определения уровня Т методом масс-спектрометрии, которые более чувствительны к низким уровням Т, чем радиоиммунный метод. С появлением этого метода появилась возможность определения нормального или повышенного уровня андрогенов в течение всей жизни женщины [18]. Имеются данные, свидетельствующие о том, что гиперпролактинемия может быть причиной гирсутизма; в связи с этим необходимы определение и контроль уровня пролактина у женщин различных возрастных групп [13]. Основным диагностическим тестом синдрома Кушинга является определение уровня свободного кортизола в суточной моче или слюне после пробы с 1 мг дексаметазона [14, 23]. Больные с аденомой надпочечников в большинстве случаев имеют нормальные показатели свободного кортизола. В связи с этим проба с дексаметазоном является идеальным тестом для выявления пациенток с субклиническими формами синдрома Кушинга [28]. После некоторых сомнений и споров в прессе по поводу того, имеются ли пороговые уровни Т и ДГЭАС, определяющие наличие опухолей яичников или надпочечников, было установлено, что при повышенных уровнях T >200 нг/дл (6,94 нмоль/л) или ДГЭАС >800 нг/мл (2171 нмоль/л) можно предполагать наличие опухолей яичников или надпочечников. Однако результаты проведенного обследования 478 женщин (в пре- и постменопаузе) с признаками и симптомами гиперандрогении противоречивы. В 11 (2-3%) случаях был выявлен высокий уровень T >250 нг/дл (8,68 нмоль/л) и только у 1 из 11 выявлена опухоль яичника. Из 10 женщин с уровнем ДГЭАС >600 нг/мл (1628 нмоль/л) у 9 была установлена опухоль надпочечника [24]. В другом исследовании, в котором принимали участие 60 женщин с диагностированной андрогенпродуцирующей опухолью яичников, у большинства из их числа уровень T колебался от 100 до 200 нг/дл (3,47-6,94 нмоль/л) [1]. Результаты данного исследования свидетельствуют о том, что андрогенпродуцирующие опухоли яичников встречаются и при уровне T ≤200 нг/дл. С целью проведения дифференциальной диагностики между опухолями яичников и надпочечников некоторые исследователи предлагают проводить 2-5-дневные тесты с минимальными дозами дексаметазона [9]. Снижение изначально повышенных уровней Т, АНД или ДГЭАС позволяет установить яичниковый генез гиперандрогении. Исследования у женщин с гиперандрогенизмом в постменопаузе весьма ограничены, в связи с этим данная проблема требует дальнейшего изучения.
Подходы к лечению постменопаузальной гиперандрогении
Методы лечения зависят от этиологии гиперандрогении. Медикаментозное и/или хирургическое лечение первичного заболевания (опухоли яичников или надпочечников, гипертекоза, ятрогенных причин, ВГКН или опухоли гипофиза) оказывает положительный эффект, проявляющийся снижением гиперандрогении. Аналоги ГнРГ могут быть использованы как в диагностических, так и в лечебных целях. Если уровни андрогенов снижаются в ответ на введение аналогов ГнРГ, опухоль считается гонадотропинзависимой; однако это не было подтверждено контролируемыми исследованиями.
Лечение гирсутизма рассмотрено в последних рекомендациях Общества эндокринологов и включает применение таких препаратов, как спиронолактон или флутамид, оказывающих антиандрогенный эффект [13]. Хотя ципротерона ацетат — прогестаген мощного антиандрогенного действия не используется для лечения гиперандрогении в США, он широко распространен в Европе [13]. Было установлено, что сенситайзеры инсулина подавляют андрогены у женщин в пременопаузе с СПКЯ [10], хотя данных об их влиянии на женщин в постменопаузе не существует.
Кардиометаболические последствия гиперандрогении. Надо ли лечить?
Данные относительно частоты и степени избытка андрогенов в период менопаузы ограничены. Нет доступной информации об отдаленных эффектах влияния избыточной продукции андрогенов на органном и системном уровне. Однако известно, что высокие уровни андрогенов нарушают липидный состав крови (повышают содержание ЛПНП, снижают уровень ЛПВП и повышают уровень триглицеридов) [25]. Недавно появились сообщения о связи конечных продуктов гликирования с уровнем Т у женщин в постменопаузе, независимо от наличия или отсутствия инсулинорезистентности [7]. Имеются также данные о повышении гематокрита у женщин с опухолями, с последующим падением его после удаления опухоли [27]. Высокий коэффициент Т/Э сопровождается усугублением инсулинорезистентности и может спровоцировать артериальную гипертензию и задержку жидкости. Исследования последних лет [8] показали, что высокие уровни Т у женщин коррелируют с повышенным риском развития рака молочной железы и заболеваниями сердца. Согласно данным L. Shaw и соавт. [21], в группе из 390 женщин, находящихся в постменопаузе с клиническими признаками ишемии, у 104 женщин с нерегулярным менструальным циклом в анамнезе и гиперандрогенией, по данным ангиограммы, чаще выявлялась ишемическая болезнь сердца, а также ожирение, метаболический синдром и сахарный диабет. Женщинам в постменопаузе с симптомами гиперандрогении необходимо проводить тщательное обследование и адекватно подобранное лечение. Тщательно собранный анамнез, физикальное обследование, лабораторные (тандемная масс-спектрометрия) и рентгенологические методы исследования позволят установить диагноз, что приведет к подбору соответствующего медикаментозного или хирургического лечения женщин с гиперандрогенией в постменопаузе.
Диета при гиперандрогении
Диетотерапия играет важную роль при основном лечении. Ведь осложнением гиперандрогении является ожирение или резкий набор веса. Врачи советуют придерживаться низкокалорийной диеты.
Нужно отказаться от простых углеводов (выпечка, сахар, сладости), от жирной пищи.
В рационе должны быть низкокалорийные белковые продукты (каша, яйца, обезжиренное молоко, творог, куриная грудка, сёмга, тунец, чечевица).
Необходимо ограничить потребление соли, пряных изделий. Алкоголь и курение препятствуют выздоровлению, поэтому от вредных привычек стоит избавиться.
При такой патологии женщина должна ежедневно употреблять не больше 85 грамм жиров и 100 грамм углеводов.
Отдавать предпочтение нужно растительной пище, так как в ее составе содержится фолиевая кислота и витамины. Они необходимы для нормальной работы пищеварительной системы и всего организма.
Для скорого выздоровления питаться нужно 4-5 раз в сутки средними порциями. Запрещено усиленно голодать, так как это только прибавит проблем эндокринной системе. Лучше обратиться к диетологу, который правильно подберет схему рациона.