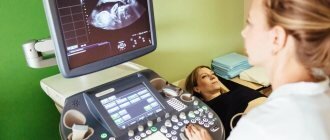
Что такое мазок на ПЦР
Полимеразная цепная реакция (ПЦР коротко) является отдельным видом молекулярно-генетической медицины. С помощью метода определяется наличие ДНК (для бактерий) и РНК (для определения вирусов).
ПРЕДУПРЕЖДЕНИЕ! Информация сайта предоставлена в ознакомительных целях, и не может использоваться для постановки диагноза, и принятия решения о лечении.
Суть метода заключается в стимулировании химических реакций в определенных условиях и с добавлением апмлификаторов.
Анализ высокочувствителен и не может дать ложноположительный результат.
Точность метода позволяет:
- установить верный диагноз;
- выявить возбудитель;
- определить стадию патологического процесса;
- провести адекватное и эффективное лечение.
ПЦР достаточно сложный анализ, требующий усидчивости и внимательности. Проводится в условиях лаборатории на современном и высокочувствительном оборудовании.
Выделяют несколько видов анализа:
- тип обратной транскрипции;
- ступенчатый;
- количественный;
- ассимметричный;
- инвертированный;
- вложенный.
Что входит в комплекс
- Вирус герпеса 1 типа, ДНК (HHV-1, ПЦР) соскоб, кол.
- Вирус герпеса 2 типа, ДНК (HHV-2, ПЦР) соскоб, кол.
- Хламидия, ДНК (Chlamydia trachomatis, ПЦР) соскоб, кол.
- Уреаплазмы, ДНК (Ureaplasma species, ПЦР) соскоб, кол.
- Микоплазма, ДНК (Mycoplasma genitalium, ПЦР) соскоб, кол.
- Микоплазма, ДНК (Mycoplasma hominis, ПЦР) соскоб, кол.
- Гарднерелла, ДНК (Gardnerella vaginalis, ПЦР) соскоб, кол.
- Трихомонада, ДНК (Trichomonas vaginalis, ПЦР) соскоб, кол.
- Гонорея, ДНК возбудителя (Neisseria gonorrhoeae, ПЦР) соскоб, кол.
- Кандида, ДНК (Candida albicans, ПЦР) соскоб, кол.
- Цитомегаловирус, ДНК (Сytomegalovirus, ПЦР) соскоб, кол.
- ВПЧ 16 типа, ДНК (HPV, ПЦР) соскоб, кол.
- Лактобактерии, ДНК (Lactobаcillus spp., ПЦР) соскоб, кол.
- ВПЧ 18 типа, ДНК (HPV, ПЦР) соскоб, кол.
Зачем беременным проходить диагностику
ПЦР при беременности является одним из обязательных видов исследований. Анализу подлежит кровь, а при необходимости, слизистый вагинальный секрет.
У беременных анализ проводится дважды – при постановке на учет по беременности и родам, и в середине заключительного триместра.
Преимущества анализа заключаются в возможности определить наличие или отсутствие вирусов, или иных микроорганизмов, вызывающих тяжелые нарушения в гестации и развитии плода.
Бактерии могут вызывать различные осложнения и негативно сказывать на развитии крохи.
Отсутствие лечения может привести к фатальным последствиям или даже явиться причиной преждевременных родов или самопроизвольного выкидыша.
Анализ ПЦР при беременности
Во время беременности любая инфекция, развивающаяся в организме матери, может повлиять на здоровье плода.
Чем скорее гинекологу удастся распознать возбудителя болезни, тем быстрее можно выбрать подходящие способы лечения.
Затягивание с устранением инфекционного процесса может привести к болезни самого малыша и даже его гибели.
Способ забора материала для анализа зависит от предполагаемого диагноза. Если у женщины наблюдается воспаление половых органов, а обычный вагинальный мазок не дает информации о возбудителе инфекции, врач порекомендует сделать мазок, который отправят на обследование методом ПЦР. Иногда рекомендуется провести и анализ крови.
Интересно! Что будет, если есть клубнику при беременности?
Если возникли подозрения, что инфекция проникла в плодные оболочки или ткани самого плода, делают анализ амниотической жидкости или ткани хориона (на более поздних сроках – плаценты). Так можно узнать о степени опасности болезни для жизни и развития малыша.
Заболевания, которые определяет анализ
Спектр параметров, которые можно выявить при помощи полимеразной цепной реакции, достаточно велик.
Сюда можно отнести:
- генетическое родство;
- хронические заболевания;
- редкие вирусные заболевания;
- грибковые инфекции;
- бактериальные процессы;
- венерические патологии.
У беременных определяются следующие патологические процессы и заболевания.
Инфекции, вызванные вирусным агентом:
- герпес;
- ВПЧ;
- цитомегаловирус;
- вирусные гепатиты В и С;
- парвовирус;
- ВИЧ инфекция;
- мононуклеоз.
Инфекции, вызванные микробами:
- уреаплазмоз;
- микоплазмоз;
- хламидиоз;
- гонорея;
- бактериальный вагиноз;
- туберкулез;
- трихомониаз.
С помощью ПЦР выявляется ВИЧ статус беременной пациентки, характер течения венерического заболевания.
Устанавливается гормональное состояние и оценивается их уровень.
Большинство неспецифических заболеваний можно диагностировать полимеразной цепной реакцией.
Это могут быть возбудители гриппа, пневмококковой инфекции, цервицита или эндометрита, а также грамм позитивные или негативные микроорганизмы, поражающие органы мочеполовой системы.
Как лечить скрытые инфекции, видео
не несет ответственности за достоверность информации, представленной в данном видео ролике. Источник — Говорит ЭКСПЕРТ
Источники:
- Ведение больных инфекциями, передаваемыми половым путём, и урогенитальными инфекциями: клинические рекомендации Российского общества дерматовенерологов и косметологов. // М.: Издательский дом «Деловой экспресс». — 2012. — С. 112.
- Диагностика и установление излеченности половых пар по урогенитальному хламидиозу и микоплазмозу. Рищук С.В., Смирнова Т.С., Костючек Д.Ф. и др. // Методические рекомендации для врачей по Северо-Западному региону России. СПб.: Медицинская пресса. — 2006. — С. 20.
- Половые пары и половые инфекции. Рищук С.В., Костючек Д.Ф. // СПб.: Медицинская пресса. — 2005. — С. 272.
- https://cyberleninka.ru/article/n/polovye-infektsii-i-reproduktivnyy-potentsial-semi
- https://cyberleninka.ru/article/n/sovremennye-metody-diagnostiki-i-lecheniya-infektsiy-peredayuschih…
- https://cyberleninka.ru/article/n/rol-infektsiy-peredavaemyh-polovym-putem-v-patologii-novorozhdenny…
Правила подготовки к анализу
Исследованию подлежит любая биологическая жидкость (кровь, моча, слюна) и вагинальный секрет.
Беременная изначально сдает венозную кровь для ПЦР диагностики:
- забор крови проводится натощак;
- за 12 часов до сдачи анализа следует отказаться от продуктов с большим содержанием жира и алкогольных напитков.
Если производится забор эпителия из влагалища, цервикального канала или уретры, перед посещением врача следует провести туалет половых органов, и исключить половые контакты накануне.
Под запретом вагинальные свечи и таблетки.
В том случае если анализу подвергается урина, ее необходимо собрать следующим образом:
- провести утренний туалет половых органов без применения мыла;
- собрать всю порцию мочи в стерильный пластмассовый контейнер;
- указать инициалы и возраст.
В некоторых бланках обязательно указывается адрес прописки или фактического места жительства.
Признаки заболевания
Несмотря на то, что наличие уреаплазмы в организме не проявляется никакими симптомами, при ее активации, приводящей к воспалениям слизистой урогенитальных органов, могут наблюдаться некоторые характерные признаки:
- болевые ощущения и рези, чувство неполного опорожнения мочевого пузыря при мочеиспускании;
- признаки общей интоксикации организма;
- субфебрильная температура;
- тянущие боли внизу живота, боли при половом акте;
- изменение выделений из влагалища в объеме (увеличение) и цвете (вместо прозрачных – слизь мутно-белого или желтого оттенка).
Как сдается
Забор крови осуществляется из вены в первой половине дня, преимущественно в утренние часы. Венозную кровь помещают в специальную вакуету для получения сыворотки.
Анализу подвергается полученная сыворотка.
Мочу доставляют в лабораторию в стерильной емкости. На проведение теста уделяется от 1 до 2 дней.
Слизистое отделяемое из влагалища собирается стерильной палочкой и помещается в стерильную среду.
Соскоб из зева шейки матки переносят на стерильное сухое предметное стекло и доставляют в лабораторию.
Если срок гестации велик, гинекологический осмотр на кресле не проводится. Беременную просят расположиться на кушетке и развести бедра.
Врач мажущими движениями собирает эпителий с поверхности мочевого канала или вводит во влагалище стерильную палочку на 2-3 см
Полученные результаты идентифицируются лечащим акушером-гинекологом. Если ПЦР проводилась с использованием мочи, результаты поступают к нефрологу или урологу.
ПЦР проводится по собственному желанию.
Ориентировочная цена зависит от спектра диагностики и выбранной методики:
- для выявления АГ или АТ к ВИЧ придется отдать около 400 рублей, а для качественного теста РНК около 4000, количественно – в пределах 11 т. р.;
- количественный вид анализа на вирусные гепатиты В и С стоит около 2000 р.;
- ЗППП – 300 р. одно заболевание, а в среднем 1500 за 5 параметров.
Что такое скрытые инфекции?
Это заболевания, вызываемые патогенной и условно-патогенной микрофлорой – простейшими, грибами, вирусами и болезнетворными бактериями. В зависимости от типа возбудителя, продолжительность инкубационного периода таких болезней варьируется: она может составлять от одной недели до года. В большинстве случаев заразившийся человек не имеет представления о носительстве и способен заражать окружающих.
Передача большинства патогенных агентов осуществляется во время половых контактов через биологические жидкости организма – слюну, сперму, вагинальный секрет и пр. Также возможна передача инфекции вертикальным путем – от беременной женщины плоду.
Мнение эксперта
Оптимальный вариант защиты от подобных инфекций – применение барьерных методов контрацепции. Однако нужно учитывать, что даже при использовании презерватива риск заражения все же остается. Поэтому рекомендуется вступать в половые контакты только с тем партнером, в здоровье которого вы уверены, а также регулярно сдавать анализы.
Врач акушер-гинеколог высшей категории Оксана Анатольевна Гартлеб
Для женщин, занимающихся сексом с одним мужчиной, в здоровье которого они не сомневаются, частота подобных обследований должна составлять не менее одного раза в год. Помимо этого, проведение обследования необходимо перед беременностью – причем пройти его должны оба партнера. Это особенно важно, если в анамнезе женщины были самопроизвольные выкидыши или замершие беременности (несостоявшиеся аборты).
Тем же, кто часто меняет половых партнеров, рекомендуется проходить обследование чаще – примерно раз в три месяца или после секса с подозрительным партнером.
Результаты исследования
Полимеразная цепная реакция позволяет определить не только присутствие патогенного агента, но и установить его количественное содержимое.
Качественные результаты исследования:
- отрицательный – в крови или в другом биологическом материале отсутствуют вирусы, бактерии или грибки. Результат не подвергается сомнению. В бланках анализов напротив исследуемого параметра ставится о или «отрицательно».
- положительный – в доставленном биологическом материале присутствуют возбудители инфекционного процесса. Обнаружение микроорганизмов свидетельствует о том, что в крови беременной (моче, слюне, слизи) присутствует ДНК или РНК. В бланке анализа делается соответствующая запись, иногда ее отмечают красной ручкой или подчеркивают для привлечения особо внимания.
При положительном тесте рекомендовано количественное определение возбудителя. От полученных результатов зависит тактика лечения и схема ведения беременной пациентки.
Выявленные венерические заболевания, становятся основанием для более тщательного контроля за состоянием плода и проведения антиретровирусной терапии.
Папилломавирусная инфекция и беременность. Особенности диагностики и тактики ведения
Распространенность папилломавирусной инфекции (ПВИ) и соответственно связанная с ней патология на протяжении последних десятилетий во многих странах мира, включая Россию, неуклонно увеличиваются. По данным литературы ежегодно в мире регистрируется до 3 млн новых случаев заражения вирусом папилломы человека (ВПЧ) [1]. Передача ВПЧ от человека к человеку может осуществляться несколькими путями: контактно-бытовым, вертикальным, при генитальных, оральных, аногенитальных контактах. Высокий рост инфицированности населения ВПЧ, обусловленный его значительной контагиозностью, многообразие вариантов патологии, ассоциированной с ним, и, главное, способность трансформировать эпителиальные клетки, запуская процесс канцерогенеза, привлекают внимание различных специалистов к поиску вариантов лечения, своевременной диагностике и профилактике заболеваний, ассоциируемых с ВПЧ [2, 3]. При этом особое внимание уделяется ПВИ урогенитального тракта, которая занимает лидирующие позиции по распространенности среди инфекций, передающихся половым путем. Активность развития и формирование ВПЧ-ассоциированной, как и другой инфекционной патологии во многом определяются состоянием иммунной системы и ее способностью адекватно реагировать на наличие патогена. Вместе с тем ВПЧ, блокируя определенные звенья иммунитета и проявляя устойчивость к ФНО-опосредованному ингибированию пролиферации, что связано со значительным снижением экспрессии ФНО-рецепторов, способен «уходить» из-под системы иммунологического надзора [4–6]. Установлено, что ВПЧ за счет активации убиквитинопосредованного протеолиза белка р53, являющегося супрессором канцерогенеза, способен влиять на механизмы регуляции молекулярно-генетического цикла деления клеток и блокировать апоптоз [7–9]. Доказано также, что белок Е7 ВПЧ нейтрализует противовирусную и противоопухолевую активность интерферона-α2 за счет его способности избирательно блокировать большинство генов, индуцируемых интерфероном [10]. Такие разнонаправленные механизмы взаимодействия ВПЧ с иммунной системой организма человека способствуют выживаемости, длительной персистенции вируса и высокому риску развития ВПЧ-ассоциированной патологии, особенно при наличии триггерных факторов.
Последовательная и целостная картина эпидемиологии и патогенеза ПВИ, сложившаяся в течение последних двух десятилетий, более четко представляется в отношении женщин, нежели мужчин [11]. ПВИ у них регистрируют в 40%, 70% и более 90% случаев рака вульвы, влагалища и шейки матки соответственно, являющихся второй по значимости причиной смерти женщин во всем мире [11–14]. В последнее время с раком цервикального канала шейки матки (95%) связывают около 20 типов ВПЧ, среди них наиболее часто выявляются ВПЧ 16-го типа (50%) и ВПЧ 18-го типа (10%) [15]. Необходимо отметить, что помимо ВПЧ в развитии онкогенной трансформации определяющую роль играет целый ряд сопутствующих факторов. Здесь прежде всего следует выделить сопутствующие инфекционные заболевания аногенитальной области. Неблагоприятна, особенно в плане развития цервикальных дисплазий, сочетанная персистенция ВПЧ с ВПГ 2-го типа, ЦМВ, ВЭБ, ВИЧ, хламидиями и микоплазмами. Особое значение, как уже было сказано выше, в возникновении инфекции, тяжести ее течения, исходе, качестве и контроле процесса терапии больных с патологией кожи и урогенитального тракта, обусловленными ВПЧ, имеет характер иммунного ответа [16].
Одной из особенностей ВПЧ-инфекции урогенитального тракта считается ее широкое распространение среди молодых женщин репродуктивного возраста, преимущественно до 25 лет [17], что обусловлено низкой сексуальной культурой населения, частой сменой половых партнеров, незащищенным сексом, вредными привычками (курение, токсикомания, алкоголизм). Отмечается рост заболеваемости детей препубертатного возраста и подростков аногенитальными бородавками, что частично можно объяснить увеличением числа детей, рано начинающих половую жизнь. По данным социологических опросов наличие половых контактов в своей жизни отметили около 15% девочек и 22% мальчиков, при этом 50% из них указали, что первый половой контакт был совершен в возрасте до 15 лет, а у 5% девочек и 20% мальчиков — до 12 лет [16]. Вместе с тем отмечено, что у подростков и молодых женщин чаще и быстрее происходит самопроизвольная элиминация ВПЧ (до 80% случаев) и регрессия имеющейся ВПЧ-ассоциированной патологии по сравнению с женщинами более позднего возраста. По результатам исследований, среднее время элиминации ВПЧ у подростков составляет 8 месяцев (CDC, 1999). По наблюдениям С. И. Роговской и В. Н. Прилепской (2006) у каждой второй пациентки в возрасте 18–25 лет этот период увеличивается до 1,5–2 лет.
Особую актуальность ВПЧ-инфекция приобретает во время беременности, при этом частота регистрации всех типов ВПЧ у беременных женщин составляет 30–65%, а типов высокого онкогенного риска — 20–30% [18].
Основная особенность беременности заключается в том, что плод по отношению к матери является генетически наполовину чужеродным (полуаллогенным) организмом, который до положенного срока не отторгается. Аллогенность плода заключается в том, что все клетки содержат помимо гаплоидного набора HLA-антигенов матери, гаплоидный набор HLA-антигенов отца. Созревание оплодотворенной яйцеклетки до зрелого плода в наполовину чужеродном организме матери осуществляется за счет супрессорного механизма, который развивается с первых часов после зачатия и действует до развития родовой деятельности. Этот механизм не позволяет иммунной системе матери осуществлять иммунную атаку на плод с целью отторжения на всех этапах его развития [19].
Развивающаяся после зачатия супрессия многофакторна и формируется как за счет продуктов эндокринной системы, так и за счет определенных изменений системных и местных иммунных реакций, выработавшихся в процессе эволюции для защиты полуаллогенного плода от иммунной системы матери: отсутствие на клетках трофобласта классических антигенов системы HLA класса I и II; сдвиг функционального баланса Т-хелперов в сторону клеток 2-го типа и иммунорегуляторная роль плаценты, обеспечивающая своеобразный иммуносупрессивный фон в организме матери [20].
Таким образом, само оплодотворение имеет под собой иммунную природу. Активные процессы, направленные на локальную иммуносупрессию, осуществляются в течение всей беременности в фетоплацентарном комплексе.
В такой ситуации ПВИ является не только высоким риском развития ВПЧ-ассоциированной патологии на фоне физиологического иммунодефицита, но и возможности передачи ее от матери к ребенку во время родов [21]. В 1989 г. доказана вертикальная передача вируса, что подтверждают сообщения об обнаружении ВПЧ в амниотической жидкости беременных и у детей, рожденных от матерей — носителей ВПЧ [22]. Возможный риск колеблется по данным разных авторов от 3% до 80% [23]. Данный разброс объясняется различиями в методике проведения полимеразной цепной реакции (ПЦР) на выявление ДНК ВПЧ. При этом ПВИ может передаваться трансплацентарно и интранатально (в частности, ВПЧ 6-го и 11-го типа). Риск инфицирования прямо пропорционален тяжести инфекции (количеству вирусных частиц) и времени безводного промежутка в родах, однако проведенные исследования свидетельствуют о том, что родоразрешение путем кесарева сечения не снижает риск инфицирования плода, что свидетельствует о преимущественно внутриутробном его заражении [22]. Интранатальное инфицирование может приводить к ювенильному рецидивирующему респираторному папилломатозу (частота составляет 1,7–2,6 на 100 000 детей и 1 на 1500 родов среди женщин с генитальной ПВИ) [24].
Инвазия вируса происходит через микроповреждения кожи и слизистых с инфицированием преимущественно незрелых, делящихся клеток базального слоя эпителия, которые являются для ВПЧ клетками-мишенями. Далее происходит репликация вируса и сборка вирусных частиц в дифференцированных клетках поверхностного слоя эпителия. При этом ВПЧ могут оказывать на эпителий продуктивное или трансформирующее воздействие. При продуктивном воздействии возникают доброкачественные новообразования — папилломы, бородавки и кондиломы кожи и слизистых оболочек. Результатом трансформирующего воздействия являются дисплазии различной степени тяжести, прогрессирующее развитие которых приводит к раку [25, 26]. Веские доказательства об ускорении развития аногенитального рака и увеличение онкологического риска при ранней экспозиции ПВИ подчеркивают особую важность не только изучения распространенности ПВИ у детей, а, главное, регулярное и длительное наблюдение за ними, учитывая возможность развития в том числе и аногенитальной неоплазии [27].
В литературе имеются исследования, доказывающие, что при подтвержденной ПЦР ПВИ у матери структурное повреждение компонентов последа в конце беременности определяется в 76,8% случаев и протекает с морфофункциональными признаками хронической плацентарной недостаточности, гипотрофии плода и осложнениями неонатального периода [28, 29].
В настоящее время отмечается увеличение и рост папилломатоза гортани как у взрослых, так и у детей. При этом у взрослых превалирует передача инфекции при ороаногенитальных контактах, а у детей при прохождении через инфицированные родовые пути и контактно-бытовым путем.
Манифестация ювенильного респираторного папилломатоза в 75–85% случаев регистрируется в первые 5 лет жизни; в 5–6% случаев у детей от 6 месяцев до года; в 45% случаев у детей до 3 лет [28].
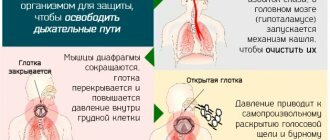
Клиническая картина респираторного папилломатоза складывается из нарушения голоса и дыхания. Наиболее часто при поражении гортани в области комиссуры и передних отделов голосовых складок развивается охриплость голоса, вплоть до полной его потери. По мере сужения просвета гортани папилломами развивается стеноз, возможна смерть от асфиксии. Патологический процесс в детском возрасте носит активный характер, для него характерны распространенность и частота рецидивирования, в связи с чем дети подвергаются многократным хирургическим вмешательствам с целью удаления папиллом. Многократная повторная эксцизия ларингеальных опухолей приводит к развитию рубцовых осложнений, необходимости трахеостомии, к потере способности говорить, усугублению хронической респираторной гипоксемии. При прогрессировании и распространении опухоли в дистальные дыхательные пути заболевание часто заканчивается фатальным исходом [24].
Учитывая, что заражение ПВИ ребенка с развитием ювенильного рецидивирующего респираторного папилломатоза возможно не только в интранатальном, а и постнатальном периоде, а также нередкую регистрацию ВПЧ-ассоциированной патологии у новорожденных и детей раннего детского возраста, следует более активно и тщательно обследовать пациентов на этапе как планирования беременности, так и во время беременности. При этом внимание уделять не только обследованию на высокоонкогенные типы ВПЧ, но и низкоонкогенные, учитывая, что, как правило, у пациентов, страдающих рецидивирующим респираторным папилломатозом, чаще обнаруживают низкоонкогенные ВПЧ 6-го и/или 11-го типа, они же нередко регистрируются и при аногенитальных бородавках и остороконечных кондиломах на других участках кожи и слизистой.
Целью исследования было оценить частоту ВПЧ-ассоциированной патологии кожи и слизистых не генитальной локализации у беременных с установленным диагнозом «аногенитальные бородавки».
Материал и методы исследования
Под наблюдением находились 76 беременных женщин (срок беременности от 12 до 26 недель) в возрасте от 18 до 42 лет с установленным клиническим диагнозом аногенитальных (венерических) бородавок. Средний возраст пациенток составил 26,3 года. У 53 (69,7%) пациентов длительность заболевания составила от 3 нед до 6 мес, у 23 (30,3%) пациентов — от 6 мес до 1 года. 18 (23,7%) пациенток констатировали о рецидивах аногенитальных бородавок после ранее проведенного лечения методами деструкции (лазерной вапоризации, электрохирургическим иссечением, криодеструкцией). Все пациентки были направлены из женских консультаций на удаление аногенитальных бородавок. Из них только у 2 (2,6%) пациенток отмечено сочетание остороконечных кондилом аногенитальной и экстрагенитальной локализации. У 42 (55,3%) больных, включенных в исследование, ПВИ подтверждалась идентификацией ВПЧ методом полимеразной цепной реакции в режиме реального времени (ПЦР-RT): ДНК ВПЧ типов 16, 31, 33, 35, 52, 58 были выявлены у 18 (42,9%) пациентов, ВПЧ типов 18, 39, 45, 59 — у 14 (33,3%), ВПЧ типов 51, 56 — у 10 (23,8%); на ВПЧ низкого онкогенного типа из них были обследованы только 6 (14,3%) пациенток: 6-й и 11-й типы обнаружены у 5 из них (11,9%). Идентификация ВПЧ методом ПЦР-RT или другим лабораторным методом не проводилась у 34 (44,7%) пациенток. Результаты исследования: при физикальном осмотре пациенток на момент их обращения за медицинской помощью у 39 (51,3%) пациенток были обнаружены остроконечные кондиломы на коже и слизистых экстрагенитальных областей: у 14 (35,9%) на коже соска и околососковой области; у 11 (28,2%) на коже конечностей; у 9 (23,1%) — на коже пупка; у 5 (12,8%) — на слизистой полости рта. В аногенитальной области папилломатозные разрастания регистрировались на коже больших половых губ — у 5 (6,6%), слизистой оболочке вульвы — у 30 (39,5%), в области задней спайки — у 4 (5,3%), на слизистой оболочке наружного отверстия уретры — у 2 (2,6%), на коже перианальной и паховых областей — у 4 (5,3%), на слизистой оболочке влагалища — у 48 (63,2%) больных. Сочетанное поражение нескольких анатомических зон аногенитальной области наблюдалось у 15 (19,7%) пациенток.
Всем пациенткам проведено удаление остроконечных кондилом радиоволновым методом. По нашим наблюдениям оптимальным сроком беременности для проведения данной процедуры определен срок гестации после 16 недель, когда заканчивается основной этап формирования плаценты и иммуносупрессивный фон в организме матери значительно снижается, что резко снижает риск возможных рецидивов.
Таким образом, нередкое обнаружение сочетанной ВПЧ-ассоциированной патологии аногенитальных и экстрагенитальных областей у беременных свидетельствует о необходимости более тщательного обследования таких пациенток с целью не только минимизации риска развития осложнений и рецидивирования ВПЧ-ассоциированной патологии, но и исключения инфицирования ребенка. Более глубокое обследование беременных на ВПЧ, включающего не только высокоонкогенные, но и низкоонкогенные типы, даст возможность избежать или значительно снизить риск развития ВПЧ-ассоциированной патологии у детей.
Литература
- Nyitray A. G., Iannacone M. R. The epidemiology of human papillomaviruses // Curr Probl Dermatol. 2014; 45 (1): 75–91.
- Семенов Д. М., Данько С. Н., Дмитраченко Т. И. Папилломавирусная инфекция (клинико-патогенетические особенности, лечение, профилактика). Учебно-методическое пособие. Витибск: Гос. мед. ун-т. СПб: Диалект. 2008. 84 с.
- Киселев В. И. Вирусы папилломы человека в развитии рака шейки матки. М.: , 2004. 180 с.
- Рахматуллина М. Р., Нечаева И. А., Шалва Марди. Опыт деструктивной терапии аногенитальных бородавок // Вестник дерматологии и венерологии. 2021. № 5. С. 96–101.
- Tavares M. C., de Lima Junior S. F., Coelho A. V. et al. // Ann Hum Biol. 2015, Jun; 16; 1–8.
- Prabhavathy D., Subramanian C. K., Karunagaran D. Re-expression of HPV16 E2 in SiHa (human cervical cancer) cell potentiates NF-kB activation induced by TNF-α concurrently increasing senescence and survival // Biosci Rep. 2015, Feb; 25; 35 (1).
- Aguilar-Martinez E., Morrisroe C., Sharrocks A. D. The ubiquitin ligase UBE3 A dampens ERK pathway signalling in HPV E6 transformed HeLa cells // PLoS One. 2015. Mar; 27; 10 (3).
- Holloway A., Simmonds M., Azad A., Fox J. L., Storey A. Resistance to UV-induced apoptosis by β-HPV5 E6 involves targeting of activated BAK for proteolysis by recruitment of the HERC1 ubiquitin ligase // Int J Cancer. 2015, Jun; 15; 136 (12): 2831–2843.
- Jing K., Shin S., Jeong S., Kim S., Song K. S., Park J. H., Heo J. Y., Seo K. S., Park S. K., Kweon G. R., Wu T., Park J. I., Lim K. Docosahexaenoic acid induces the degradation of HPV E6/E7 oncoproteins by activating the ubiquitin-proteasome system // Cell Death Dis. 2014, Nov; 13; 5: 1524.
- Сухих Г. Т., Прилепская В. Н., Роговская С. И. и др. Применение препаратов интерферона при лечении плоскоклеточных интраэпителиальных поражений шейки матки низкой степени // Эффективная фармакотерапия в акушерстве и гинекологии. 2009. № 4. С. 36–41.
- Батыршина С. В., Шулаев А. В., Акберова Д. Р. Папилломавирусная инфекция: оптимизация диагностики и лечения // Клиническая дерматология и венерология. 2015. 14 (5). С. 67–77.
- Baldwin A., Pirisi L., Creek K. E. NFI-Ski interactions mediate transforming growth factor beta modulation of human papillomavirus type 16 early gene expression // J Virol. 2004, Apr 1; 78 (8): 3953–3964.
- Byg L. M., Vidlund J., Vasiljevic N. et al. NF-kB signaling is attenuated by the E7 protein from cutaneous human papillomaviruses // Virus Res. 2012, Oct 1; 169 (1): 48–53.
- Grulich A. E., Jin F., Conway E. L. et al. Cancers attributable to human papillomavirus infection // Sex Heath. 2010; 7 (3): 244–252.
- Данилова О. В., Юнусова Е. И. Тактика ведения папилломавирусных поражений гениталий. Учебное пособие для врачей. Казань, 2012. 30 с.
- Юнусова Е. И., Данилова О. В., Гизатуллина Р. Д. ВПЧ-ассоциированная патология урогенитального тракта. Сборник материалов V Всероссийской научно-практической конференции с международным участием «Казанские дерматологические чтения: синтез науки и практики. Казань, 2021. С. 117–121.
- Ван Крог Д., Лейси С. Д., Гросс Д., Баракко Р., Шнайдер А. Европейское руководство по аногенитальным бородавкам // ИППП. 2002. № 3. С. 29–37.
- Szepietowska M., Sfodzifski H. et al. Evaluation of frecuency HPV infection during pregnancy // Ginecol Pol. 2002; 73 (8): 662–665.
- Долгушина Н. В. Иммунологические аспекты развития плацентарной недостаточности и невынашивания беременности у пациенток с хроническими вирусными инфекциями // Акушерство и гинекология. 2008. № 4. С. 16–19.
- Wicherek L., Basta P., Sikora J. at al. RCAS1 decidual immunoreactivity in servere pre-eclampsia: Immune cell pre-cence and activity // Amer. J. Period. Immunol. 2007. V. 68, № 4. P. 358–366.
- Woodhall U. K., Jeet M., Soldan K. et al. Effect of genital warts: the loss of guality of life and cost of treatment in eight sex clinics in the UK // Sex and the transmissions. 2011; 87: 458–463.
- Sedlacek T. V., Lindheim S. et al. Mechanism for HPV transmission at birth // Am J Obstet Gynecol. 1989; 161: 55–59.
- Watts D. H., Koutsky L. A. et al. Low — risk perinatal transmission of HPV: results from a prospective cohort study // Am J Obstet Gynecol. 1989; 178: 365–373.
- Green G. E., Bauman N. M., Smith R. J. Pathogenesis and treatment of juvenile onset recurrent respiratory papillomatosis // Otolaryngol Clin North Am. 2000; 33 (1): 187–207.
- Роговская С. И. Папилломавирусная инфекция у женщин и патология шейки матки. М.: ГЕОТАР-Медиа, 2005. С. 15–17.
- Юнусова Е. И., Юсупова Л. А., Мавлютова Г. И., Гараева З. Ш. Плоские бородавки: особенности и возможности терапии // Лечащий Врач. 2021. № 5. С. 52–55.
- Коколина В. Ф., Малиновская В. В. Папилломавирусная инфекция. Пособие для врачей. М., 2008. 44 с.
- Воробцова И. Н., Тапильская Н. И., Гайдуков С. Н. Результаты обследования новорожденных, рожденных от матерей с различными формами папилломавирусной инфекции // Педиатр. 2011. Т. II. № 4. С. 72–75.
- Чистяков М. А. Патоморфология папилломавирусной инфекции в системе «мать-плацента-плод». Автореф. дис. … к.м.н. М., 2008. 25 с.
Е. И. Юнусова1, кандидат медицинских наук О. В. Данилова, кандидат медицинских наук Л. А. Юсупова, доктор медицинских наук, профессор Г. И. Мавлютова, кандидат медицинских наук З. Ш. Гараева, кандидат медицинских наук
ГБОУ ДПО КГМА МЗ РФ, Казань
1 Контактная информация
Папилломавирусная инфекция и беременность. Особенности диагностики и тактики ведения/ Е. И. Юнусова, О. В. Данилова, Л. А. Юсупова, Г. И. Мавлютова, З. Ш. Гараева Для цитирования: Лечащий врач № 5/2018; Номера страниц в выпуске: 56-59 Теги: папилломавирусная инфекция, поражение кожи, половой путь распространения
Преимущества анализа
Гестационный период может быть осложнен внутриутробной инфекцией, выявить и устранить которую бывает непросто. Коварство ВУИ заключается в отрицательном влиянии на состояние здоровья развивающегося плода.
Инфекции становятся причиной инфицирования ребенка, ухудшают его развитие. Часто становятся причиной внутриутробных аномалий несовместимых с жизнью.
Гинекологи рекомендуют внимательно относится к своему здоровью и проходить все рекомендованные процедуры.
Анализ на выявление инфекций с помощью ПЦР метода зарекомендовал себя только с положительной стороны:
- во-первых, полученные результаты действительны на 100 %;
- во-вторых, инфекция идентифицирована качественно и количественно;
- в-третьих, четко определяется степень формации и серьезность патологии.
Метод точен и эффективен. Из минусов – высокая стоимость.
Не все виды анализов на инфекции включены в перечень ОМС, поэтому возникает необходимость обращаться в частные организации.
Например, вирус Эпштейна-Барра можно выявить только при помощи цепной ступенчатой реакции. Его стоимость в частных лабораториях будет колебать от 900 до 1300 рублей.
Немаловажным преимуществом является быстрота исследования. Результаты получают в день сдачи биологического материала, либо на следующий день.
Своевременное выявление возбудителя максимально снижает риск заражения плода во внутриутробном периоде. Кроме того, гинекологи продумывают лечение по результатам ПЦР диагностики.
Опасность самолечения
Самолечение опасно при любой симптоматике, но занимаясь самолечением в ожидании ребенка, женщина рискует не только своим здоровьем, но и здоровьем будущего малыша.
При клинической картине воспалительного процесса мочеполовых органов при самолечении обычно прибегают к помощи антибиотиков или антивирусных препаратов. Опасность такого бессистемного приема препаратов может привести к еще более активному росту микроорганизмов, вызвавших воспалительный процесс. Ведь «прописывая» себе лечение самостоятельно, женщина не знает, какой агент вызвал воспаление. Антивирусные препараты подавят или уничтожат не бактерии, к которым относится уреаплазма, а вирусы, увеличив тем самым в составе микрофлоры болезнетворные в данный момент микроорганизмы.
Но даже антибиотик для самолечения будет выбран с ошибкой, поскольку только специалист знает, какой из множества этих препаратов подходит для лечения каждого вида бактерии.
Беременная обязана внимательно следить за состоянием своего организма, чтобы заметить малейшие отклонения и своевременно обратиться за медицинской помощью в ближайшее гинекологическое отделение сети клиник НИАРМЕДИК, чтобы опытные врачи-гинекологи предотвратили развитие патологий, представляющих опасность для здоровья женщины и будущего малыша.
Популярные вопросы
3 день жжение, после того, как схожу в туалет. Выделения бело желтого цвета.
Здравствуйте! Порекомендую воспользоваться гелем Гинокомфорт восстанавливающим, по 1 дозе 1 раз в день 5 — 7 дней. Если не отметите улучшения, то обратитесь на приём к урологу для проведения обследования и коррекции терапии.
Жжение после ежедневок, реакции на ежедневки, боль при мочеиспускании и жжение, как будто мочевой полный, хожу в туалет каждые 5 мин, скажите, что делать?
Здравствуйте! В данной ситуации важно чтобы инфекция не распространилась дальше из уретры в мочевой пузырь и почки. Порекомендую местно воспользоваться гелем Гинокомфорт восстанавливающим, обильное питьё 2 литра, урологический сбор. А, главное, как можно скорее сдать общий анализ мочи и проконсультироваться с урологом на предмет приёма антибактериальных препаратов.
Здравствуйте! У меня инфекции половых путей, можно ли лечить это, и каким образом?
Здравствуйте! Прежде всего, Вам необходимо обратиться к врачу и провести обследование на выявление инфекционного фактора. Это позволит грамотно назначить основную терапию. В дополнение для улучшения и закрепления эффекта лечения можно будет в схему подключить гель Гинокомфорт с маслом чайного дерева по 1 дозе 1 раз в день 7-10 дней.
Здравствуйте, скажите пожалуйста по всем инфекциям написано: не выявлено, а уреаплазма: 10*2.7. Норма ли это?
Здравствуйте! Уреаплазмы относятся к инфекциям, передающимся половым путем. Микробное число может меняться при снижении иммунитета, а также инфицировать партнёра. Выявленная инфекция требует проведения лечения.
Для точной диагностики обращайтесь к специалисту