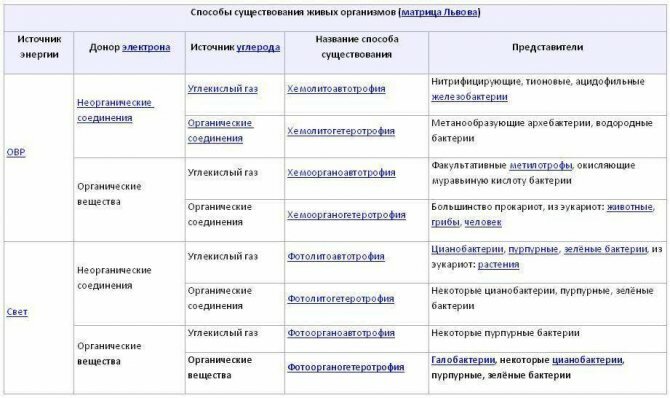
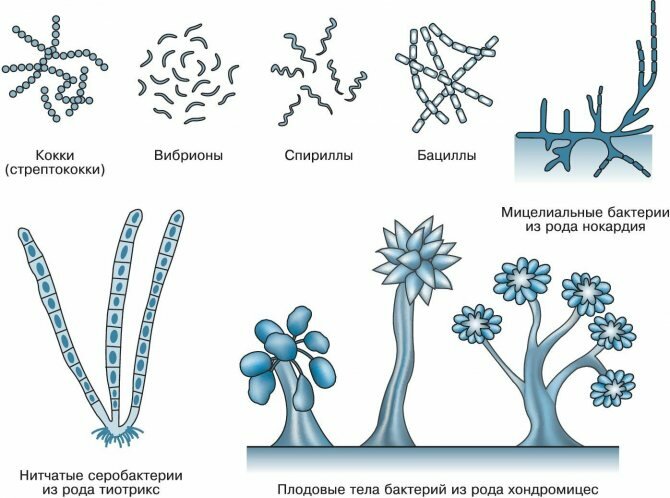
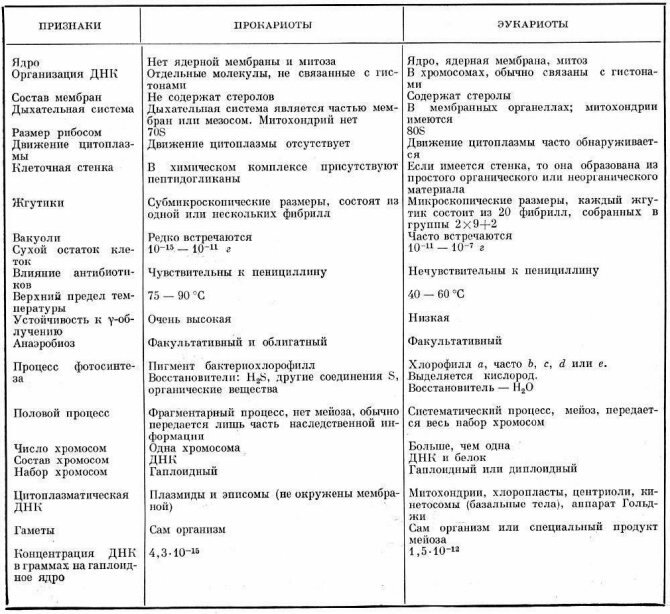
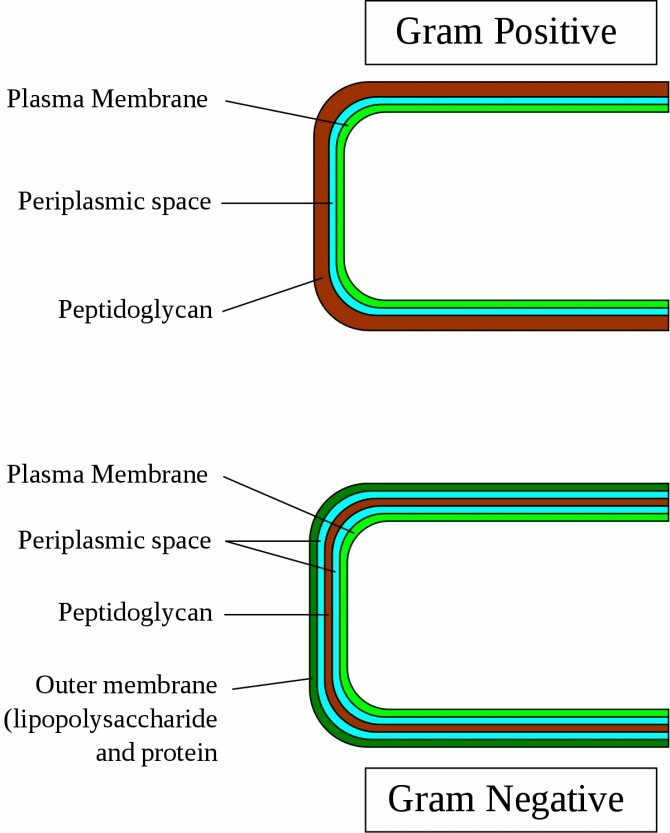
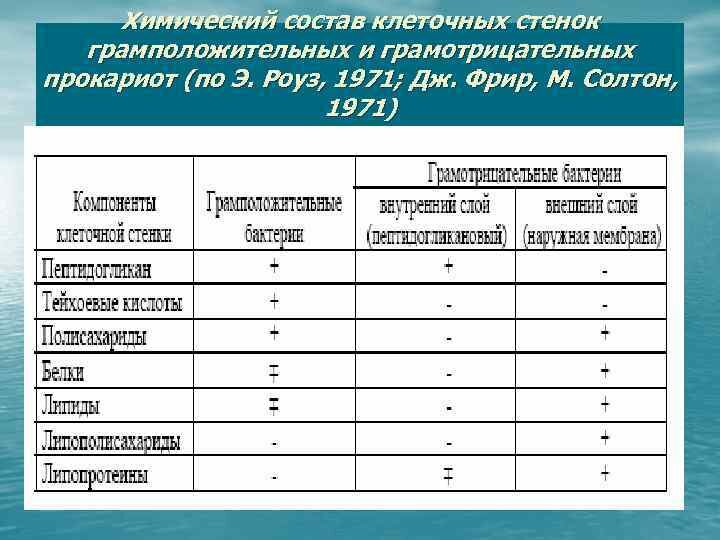
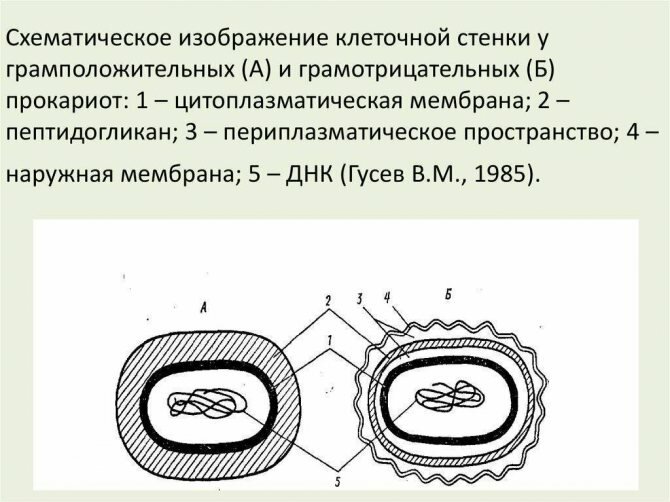
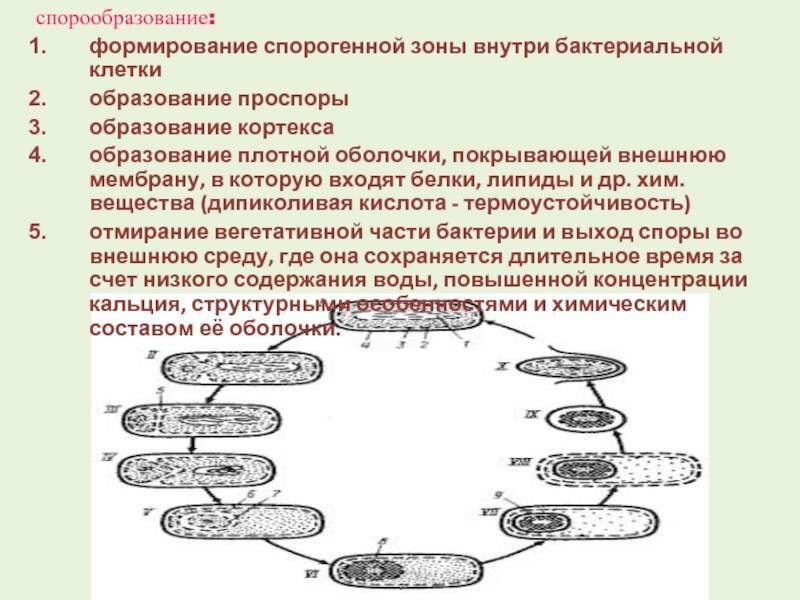
09 Октября 2020
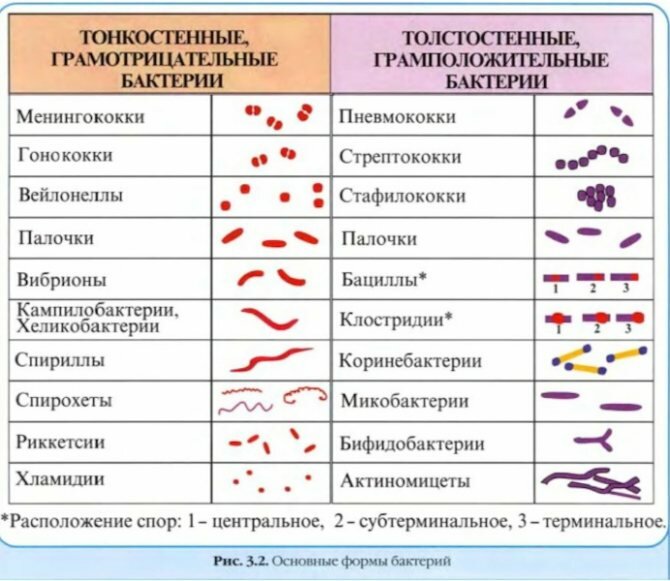
Существуют две больших группы бактерий — грамположительные и грамотрицательные. Название происходит от их способности к окрашиванию по методу Грама. Этот метод назван в честь самого разработчика Х. К. Грама, который открыл метод в 1884 году. А уже в 1886 году Эмиль Ру доказал, что не все бактерии окрашиваются одинаково и тогда произошло это разделение по классам. Отличие состоит в строении клеточной стенки. Этот лабораторный анализ до сих пор является стандартом для дифференцировки бактерий в микробиологии.
Основные виды грамположительных бактерий
Большинство опасных для человека микроорганизмов – грамположительные бактерии. Они вызывают такие заболевания, как ботулизм или столбняк, эти болезни плохо поддаются лечению. Кроме того, микоплазму, которую не относят к этому типу, также произвели на свет грамположительные бактерии.
Виды грампозитивных микроорганизмов:
- кокки: клетки, соединенные между собой с помощью целлюлозы; в основном это анаэробные молочнокислые стрептококки;
- палочки: спорообразующие представлены анаэробными клостридиями; не способные образовывать споры – молочнокислые лактобациллы;
- коринеморфы: отличаются склонностью к изменению формы – это стрептомицетовые и пропионовокислые бактерии.
Подобные микроорганизмы вызывают массу недугов. Стафилококки провоцируют грибковые инфекции. Особенно опасен золотистый стафилококк.
Стрептококковые микроорганизмы вызывают фарингиты, рожу, реже пневмонию, сепсис.
Энтерококки часто поражают мочевыводящие пути, сердечную мышцу и провоцируют нагноения в ранах.
Заражение пневмококком зачастую проходит в сопровождении острых симптомов. Синуситы, отиты, внезапные генерализированные пневмонии – вот список заболеваний, вызванных этим возбудителем.
Что касается палочек, то самая известная из них – дифтерийная палочка, выделяющая смертельно опасные токсины и относящаяся к коринебактериям. Помимо нее, палочками вызываются сибирская язва и ботулизм.
Газовую гангрену вызывают бактерии под названием клостридии. Заболевание столбняком также обязано своим существованием этому виду бактерий. Причем столбнячные споры очень живучи: выдерживают длительное кипячение и замачивание в дезинфицирующих растворах.
Чем опасны
Хотя хороших микроорганизмов гораздо больше, чем плохих, некоторые бактерии вредны. При контакте человека с вредоносными организмами они могут попасть в тело, где начинают быстро размножаться, выделять токсины, которые повреждают ткани тела, вызывая недомогание.
Плохие бактерии называются патогенными, потому что они вызывают заболевания, такие как ангина, стафилококковые инфекции, холера, туберкулез и пищевые отравления.
Некоторые виды грамположительных бактерий способны вызывать серьезные инфекционные заболевания:
- Инфекции мочевыводящих путей.
- Туберкулез.
- Дифтерию.
Инфекций, вызываемые грамотрицательными бактериями:
- Пневмония.
- Менингит.
- Перитонит.
- Инфекции крови.
Мир бактерий
Царство микроорганизмов настолько разнообразно и сложно устроено, что даже современная наука еще не изучила его полностью. Есть такие бактерии, которые выживают при высоких температурах и не погибают даже при длительном кипячении, другие же гибнут при малейшем изменении температуры или состава внешней среды, например после добавления обычного сахара. Некоторые микроорганизмы прекрасно себя чувствуют в горячих источниках, в кислоте, питаются метаном или другими химическими веществами.
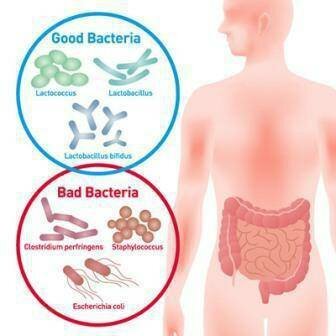
Бактерии – это самые древние организмы и очень широко распространены в мире. Они встречаются везде: на дне океана, в воздухе, в почве – даже на большой глубине, в организме живых существ. Причем, наукой доказано, что клеток бактерий внутри человека в 10 раз больше, чем собственных. Некоторые микроорганизмы просто живут рядом с другими живыми существами, другие же активно с ними взаимодействуют. Они могут приносить пользу или вызывать различные заболевания. Причем полезных бактерий в десятки раз больше, чем патогенных.
Многие микроорганизмы приносят пользу. Например, те, которые обитают в кишечнике человека, участвуют в пищеварении и защищают его от инфекций. Это лактобактерии и бифидобактерии. В полости рта человека обитает около 40 млн видов бактерий, но всего 5 % из них патогенные. Есть микроорганизмы, которые участвуют в разложении отходов. Но, несмотря на то что полезных бактерий все же больше, патогенные их виды приносят много вреда, так как вызывают опасные болезни. До сих пор много человек во всем мире умирает от туберкулеза, холеры, столбняка, брюшного тифа, ботулизма и других инфекций
Поэтому очень важно научиться правильно взаимодействовать с миром бактерий
Зачем нужны
Есть много видов бактерий, которые приносят пользу человеку:
- Микробы в кишечнике расщепляют многие из белков, липидов и углеводов на питательные вещества, которые затем человек усваивает. Более того, микробы производят полезные соединения, такие как витамины и противовоспалительные средства, которые геном человека не может производить. Миллионы бактерий населяют пищеварительную систему человека, которые помогают переваривать пищу и производить жизненно важные витамины, такие как биотин и витамин К.
- Бактерии в кишечнике работают с иммунной системой, защищая организм от заболеваний.
- Микроорганизмы, находящиеся внутри желудка, помогают поддерживать уровень pH и кислотности в желудке.
- Защищают кожу. Множество бактерий на коже (почти 200 различных видов у здорового человека) контролируют окружающую среду кожи и ее ресурсы, не давая другим вредным микробам закрепляться.
- Полезные бактерии, способные производить кислород, используют для создания антибиотиков.
- Бактерии используются в производстве продуктов питания для приготовления йогуртов и ферментированных продуктов.
Где встречается грамотрицательная флора, и какой она бывает
Мир полон микробов. Это утверждение на 100% соответствует распространению этой флоры. Существует множество семейств грамотрицательных кокков (шаровидных микробов) и палочек.
К ним относят, в том числе:
- псевдомонады. Они применяются в химической и микробиологической промышленности, как продуценты многих органических кислот и соединений;
- Моракселлы;
- ацинетобактерии;
- флавобактерии.
Непосредственно заболевания у человека вызывают сальмонеллы (сальмонеллез, брюшной тиф), шигеллы (дизентерию), легионеллы. Наиболее яркими представителями патогенной флоры являются нейссерии, вызывающие гонорею и менингит. Они относятся к диплококкам. Грамотрицательными являются гемофильные палочки, геликобактер пилори, энтеробактер и протей.
Эти микроорганизмы обладают общей способностью сохранять углеводную лабораторную среду, вследствие слабой ферментативной активности. Эти неферментирующие сахар грамотрицательные бактерии находятся повсюду. Они встречаются в почве, в воде, попадают на пищевые продукты. Испражнения человека и животных также сдержит большое количество этих микроорганизмов. Они находятся на коже, в верхних дыхательных путях.
Существуют полезные грамотрицательные микробы: так, азотфиксирующие клубеньковые бактерии на корнях бобовых растений, которые обогащают почву азотом, также относятся к данному виду микробной флоры. К грамотрицательной флоре относятся и метановые бактерии, которые в качестве единственно возможного источника пищи рассматривает СН4, или метан. Некоторые кокки и палочки относятся к факультативным анаэробам, то есть для их роста и размножения вовсе не обязательно присутствие кислорода воздуха.
Какие заболевания вызывают
При определенных условиях грамотрицательные бактерии становятся причиной серьезных болезней. Связано это с тем, что сложная оболочка этих микроорганизмов при разрушении выделяет много токсинов, которые, разносясь по кровотоку человека, вызывают сильнейшую интоксикацию. Получается, что патогенны не сами бактерии, а особенности их клеточной оболочки — липополисахаридный слой, который вызывает иммунную реакцию организма. Они приводит к развитию воспаления. Но если у человека иммунитет в порядке, он легко справляется с такими микроорганизмами, и инфекция ему не страшна.
К грамотрицательным бактериям относятся микроорганизмы, вызывающие гонорею, сифилис, менингит и респираторные заболевания. Особенно распространены такие бактерии, котрые вызывают поражение дыхательных и мочевыделительных путей, желудочно-кишечного тракта. К грамотрицательным относятся такие известные возбудители инфекций, как протей, эшерихия, энтеробактерии, сальмонеллы. Они вызывают сальмонеллез, менингит, брюшной тиф, дизентерию. Кроме того, именно такие устойчивые микроорганизмы являются причиной тяжелых внутрибольничных инфекций. Ведь они могут выжить даже после серьезной дезинфекции.
Как бороться с грамотрицательными бактериями
Как было сказано выше, грамположительные микробы имеют проницаемые клеточные стенки. К ним относятся все спорообразующие кокки, в том числе стафилококки и стрептококки, бациллы и листерии, клостридии и микобактерии. Наибольшую опасность представляет золотистый стафилококк, который при поражении ослабленного организма способен угрожать жизни больного.
Грамположительные микробы способны поразить головной мозг и сердце, дыхательные пути и кровь, а также стать причиной гнойной инфекции в ранах. Именно такие бактерии становятся причиной распространенных инфекций, в частности:
- дифтерии;
- отита и синусита;
- пневмонии;
- сибирской язвы;
- фарингита и тонзиллита;
- воспаления мозга;
- заражения крови;
- ботулизма;
- газовой гангрены;
- столбняка;
- пищевой токсикоинфекции.
Эти патогенные микроорганизмы распространены не меньше грамположительных бактерий. Список их довольно многообразный, причем среди них встречаются такие, которые являются условно-патогенными, а значит, в обычных условиях не причиняют никакого вреда человеку. Наиболее распространенными грамотрицательными бактериями считаются:
- менингококки;
- псевдоманады;
- протеобактерии;
- спирохеты;
- бруцеллы;
- хеликобактерии;
- гонококки.
Здесь следует понимать, что оболочка этих микроорганизмов выделяет много вредных токсинов, которые провоцируют сильнейшее отравление организма. Выходит, что в патогенности виноваты не сами микробы, а особенность строения их внешней оболочки, того самого липополисахаридного слоя, который и провоцирует тяжелую интоксикацию и воспалительный процесс в организме.
При распространении в организме грамотрицательные бактерии способны вызвать менингит, сифилис и гонорею, гастрит и язву желудка, а также различные респираторные заболевания.
Кроме того, в группу грамотрицательных бактерий следует включить энтеробактерии, протеи, сальмонеллы и эшерихии коли, которые могут провоцировать кишечную инфекцию, дизентерию, брюшной тиф и сальмонеллез. Именно эти патогенные микроорганизмы становятся причиной тяжелых внутрибольничных инфекций, ведь они способны выживать даже после серьезной дезинфекции (а некоторые продолжают существовать даже после трехдневного кипячения). Врачи находят их в бронхоскопах и ларингоскопах, на нестерильных повязках и в масках наркозной аппаратуры.
А ведь кроме устойчивости к дезинфицирующим средствам, грамотрицательные бактерии «славятся» серьезной лекарственной устойчивостью.
Как можно догадаться, и сегодня, спустя более 100 лет, для успешного лечения инфекционных заболеваний широко используется метод Грама. Он позволяет быстро и эффективно определить, какие именно бактерии вызвали болезнь – грамотрицательные или грамположительные. В зависимости от этого больному подбирают антибактериальные препараты.
Однако выявить возбудителя инфекции гораздо легче, чем бороться с ним. Столкнувшись с заболеваниями, вызванными грамотрицательными бактериями, врачи обычно назначают не один, а сразу два антибиотика или же прописывают антибактериальные средства широкого спектра действия. Против таких микробов может быть эффективен Амоксициллин или Ампициллин, Стрептомицин или Хлорамфеникол.
Столкнувшись с грамотрицательной микрофлорой, специалисты всегда должны комбинировать антибиотики различных групп, держа при этом наготове препараты резерва. Особенно это касается сложных госпитальных инфекций, которые не всегда можно вылечить одним, даже современным антибиотиком.
В заключение статьи хочется напомнить всем читателям, что грамотрицательные бактерии являются условно-патогенными микроорганизмами, которые поражают организм только в том случае, если сильно снижается иммунитет. Это могут быть периоды восстановления после тяжелых заболеваний или операций, наличие хронических болезней или же ВИЧ-инфекции.
В этом плане каждый человек, который часто простужается, имеет инфекционные или гнойничковые заболевания, должен обратить внимание на состояние иммунной защиты организма. Своевременно принятые меры по укреплению иммунитета позволят вам избежать неприятного знакомства с этой условно-патогенной микрофлорой.Берегите свое здоровье!
Заболевания, которые они вызывают
Именно грамположительные бактерии являются причиной таких распространенных инфекционных болезней, как:
- тонзиллит, фарингит;
- синусит, отит;
- ревматизм;
- заражение крови;
- пневмония;
- воспаление мозга;
- сибирская язва;
- пищевые токсикоинфекции;
- ботулизм;
- дифтерия;
- столбняк;
- газовая гангрена.
Грамположительные и грамотрицательные бактерии
В нашем организме содержатся как грамположительные, так и грамотрицательные микроорганизмы. Их правильное соотношение позволяет поддерживать работу многих органов, в частности, микрофлору кишечника, влагалища или полости рта. Сохранение баланса этих микробов становится надежной защитой от инфекций.
Грамположительная флора
Как было сказано выше, грамположительные микробы имеют проницаемые клеточные стенки. К ним относятся все спорообразующие кокки, в том числе стафилококки и стрептококки, бациллы и листерии, клостридии и микобактерии. Наибольшую опасность представляет золотистый стафилококк, который при поражении ослабленного организма способен угрожать жизни больного.
Грамположительные микробы способны поразить головной мозг и сердце, дыхательные пути и кровь, а также стать причиной гнойной инфекции в ранах. Именно такие бактерии становятся причиной распространенных инфекций, в частности:
- дифтерии;
- отита и синусита;
- пневмонии;
- сибирской язвы;
- фарингита и тонзиллита;
- воспаления мозга;
- заражения крови;
- ботулизма;
- газовой гангрены;
- столбняка;
- пищевой токсикоинфекции.
Грамотрицательные бактерии
Эти патогенные микроорганизмы распространены не меньше грамположительных бактерий. Список их довольно многообразный, причем среди них встречаются такие, которые являются условно-патогенными, а значит, в обычных условиях не причиняют никакого вреда человеку. Наиболее распространенными грамотрицательными бактериями считаются:
- менингококки;
- псевдоманады;
- протеобактерии;
- спирохеты;
- бруцеллы;
- хеликобактерии;
- гонококки.
Эти микробы устойчивы ко многим антибиотикам, а потому лечить заболевания, вызванные такой микрофлорой, чрезвычайно трудно. Какие же патологии, вызывают грамотрицательные микроорганизмы?
Здесь следует понимать, что оболочка этих микроорганизмов выделяет много вредных токсинов, которые провоцируют сильнейшее отравление организма. Выходит, что в патогенности виноваты не сами микробы, а особенность строения их внешней оболочки, того самого липополисахаридного слоя, который и провоцирует тяжелую интоксикацию и воспалительный процесс в организме.
При распространении в организме грамотрицательные бактерии способны вызвать менингит, сифилис и гонорею, гастрит и язву желудка, а также различные респираторные заболевания.
Кроме того, в группу грамотрицательных бактерий следует включить энтеробактерии, протеи, сальмонеллы и эшерихии коли, которые могут провоцировать кишечную инфекцию, дизентерию, брюшной тиф и сальмонеллез. Именно эти патогенные микроорганизмы становятся причиной тяжелых внутрибольничных инфекций, ведь они способны выживать даже после серьезной дезинфекции (а некоторые продолжают существовать даже после трехдневного кипячения). Врачи находят их в бронхоскопах и ларингоскопах, на нестерильных повязках и в масках наркозной аппаратуры.
А ведь кроме устойчивости к дезинфицирующим средствам, грамотрицательные бактерии «славятся» серьезной лекарственной устойчивостью.
Грамположительная флора
Большинство бактерий, которые поддаются окрашиванию фиолетовым красителем, то есть имеют проницаемую клеточную стенку, опасны для человека. К ним относятся стрептококки, стафилококки, листерии, бациллы, клостридии, микобактерии, актиномицеты. Особенно опасен золотистый стафилококк, который поражает ослабленный организм и без лечения быстро приводит к смерти больного. Но к ним относятся также полезные молочнокислые лактобактерии.
Грамположительные микроорганизмы поражают дыхательные пути, сердечную мышцу, головной мозг, кожу. Они провоцируют гнойную инфекцию в ранах, заражение крови.
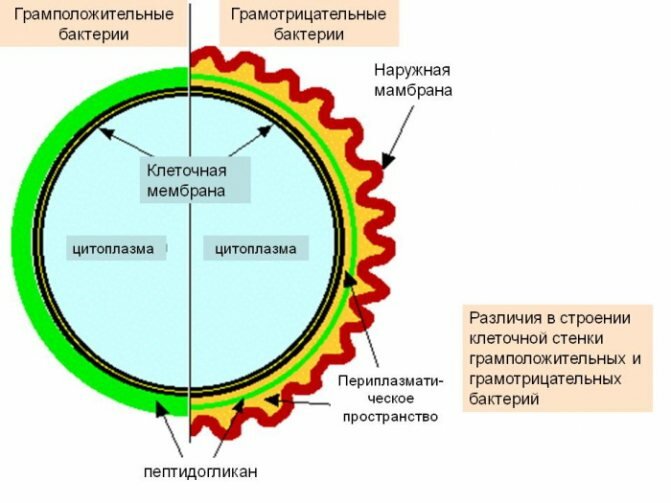
Характеристика
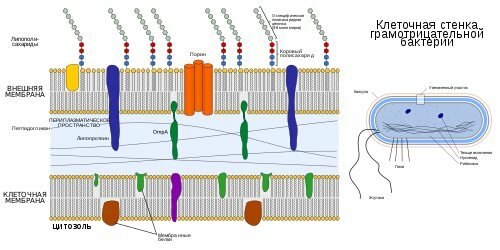
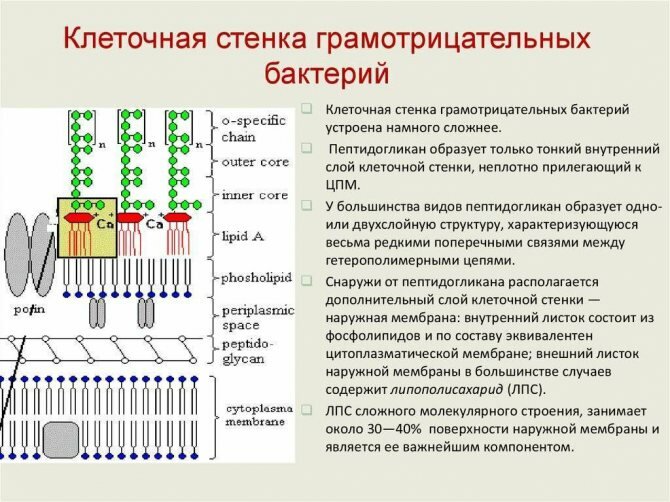
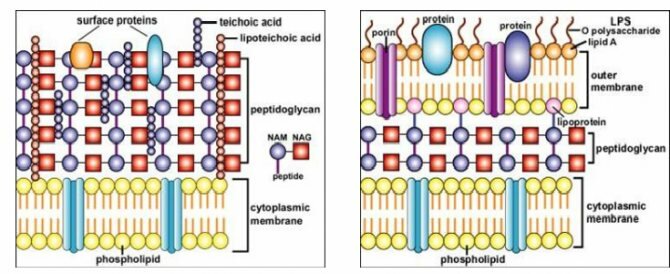
Строение оболочки клетки грамотрицательных бактерий
Общие признаки, свойственные большинству грамотрицательных бактерий:
- Наличие двух мембран, между которыми находится клеточная стенка и периплазматическое пространство.
- Более тонкий, по сравнению с грамположительными бактериями, пептидогликановый слой.
- Наружная мембрана содержит липополисахариды (состоит из липида А, полисахаридного ядра и антигена О снаружи и из фосфолипидов изнутри).
- В наружной мембране присутствуют порины, функционирующие подобно порам для определённых молекул.
- S-слой прикреплен к наружной мембране, а не к пептидогликановому слою.
- Если есть жгутик, он имеет четыре поддерживающих кольца, а не два.
- Отсутствуют тейхоевая и липотейхоевая кислоты.
- Обычно не образуют спор (примечательным исключением является Coxiella burnetii
, образующая спороподобные структуры). - Липопротеины прикреплены непосредственно к полисахаридной основе.
- Большинство содержат липопротеин Брауна, который связывает наружную мембрану и цепочки пептидоглюканов ковалентной связью.
Главная / Издательство / Патогенез грамположительного и грамотрицательного сепсиса
2.2.4. Патогенез грамположительного и грамотрицательного сепсиса
Грамположительные микроорганизмы не содержат в клеточной стенке эн-дотоксина, имеют липополисахаридную капсулу, их клеточная стенка содер-жит фосфолипидную мембрану, окруженную слоем пептидогликанов. Каж-дый из этих слоев может содержать такие полимеры, как тейхоновая, тейху-роновая кислоты, полисахариды. На поверхности клеток располагаются спе-цифические антигены, такие как стафилококковый протеин А, стрептококко-вый протеин М. Развитие септического ответа индуцируют гликоколикс грамположительной микрофлоры, предшественники пептидогликана и дру-гие компоненты клеточной стенки. Установлено, что предшественники пеп-тидогликана и другие компоненты клеточной стенки индуцируют продукцию таких медиаторов воспаления, как ФНО, ИЛ-1. Пептидогликаны и тейхоно-вая кислота активируют альтернативные пути активации комплемента, изме-няют активность макрофагов и лимфоцитов (Р.Бэлк, 1994). Комплекс ответ-ных реакций на инвазию грамположительной инфекции является более сложным по сравнению с таковыми при эндотоксикозом. В то же время от-мечаются и общие с эндотоксикозе закономерности формирования метабо-лических и функциональных расстройств.
В настоящее время идентифицировано большое количество токсинов грамположительной микрофлоры, реализующих свои эффекты через индук-цию цитокинов, воспалительных лейкотриенов, простагландинов, а также че-рез каскад реакций активации системы комплемента, тромбоцитарного звена системы гемостаза, коагуляционного гемостаза и фибринолиза. Одним из токсинов, выделенных при грамположительном сепсисе, является токсин-1, который, действуя подобно эндотоксину, вызывает синдром септического шока, инициирует системный воспалительный ответ.
Подобно грамотрицательным бактериям грамположительные бактерии за счет продуцируемых ими токсических субстанций повышают проницаемость сосудистой стенки, активируют моноциты, лимфоциты, полиморфноядерные лейкоциты, тромбоциты и другие клетки, повышают проницаемость цито-плазматических мембран, вызывая развитие цитолиза.
Ведущая роль в развитии грамотрицательного сепсиса отводится эндоток-сину.
Как известно, эндотоксины продуцируются различными грамотрицатель-ными бактериями, в частности, кишечной палочкой, протеем, сальмонелла-ми, шигеллами, менингококком и другими возбудителями инфекций.
Установлено, что клеточная оболочка грамотрицательных бактерий имеет три слоя: внутренний (цитоплазматическая мембрана), средний слой (плот-ная мембрана, пептидогликановый слой) и наружный слой (наружная мем-брана, представленная липопротеидами и липополисахаридами). Липидные компоненты в наружной мембране расположены асимметрично: фосфолипи-ды находятся преимущественно внутри, а липополисахариды (ЛПС) локали-зованы во внешней части наружной мембраны (Езепчук Ю.В., 1985). ЛПС как поверхностная структура бактериальной клетки включает О-антигены, несущие в себе сайты связывания для антибактериальных антител, рецепто-ры для бактериофагов. ЛПС влияют на рост и жизнедеятельность грамотри-цательных бактерий. В то же время ЛПС у человека и животных вызывает выраженный эндотоксический эффект.
ЛПС, выделенный из различных видов бактерий, состоит из гетеро-полисахаридной части, которая ковалентно связана с липидным компонен-том, названным липидом А. Эти две части детерминируют различные свой-ства ЛПС.
Гетерополисахаридная часть (О-специфические боковые цепи и ядро) не-сет структуры, которые распознаются лектинами, специфическими антите-лами и бактериофагами. Другая функционально важная часть ЛПС – липид А – ответственна за эндотоксический эффект. Липид А, выделенный из ЛПС различных грамотрицательных бактерий, имеет идентичную организацию и обладает стереотипными биологическими эффектами, в частности, пироген-ностью, летальной токсичностью, иммуногенностью, митогенностью, связы-вается с мембраной клеток эукариотов, стимулирует альтернативный путь активации комплемента, систему мононуклеарных фагоцитов, освобождение макрофагами лизосомальных ферментов, монокинов, токсических радикалов кислорода, оксида азота, активирует прокоагулянтную систему и систему фибринолиза.
Помимо эндотоксина в развитии грамотрицательного сепсиса определен-ная роль отводится экзотоксинам.
Патогенез сепсиса и септического шока. В настоящее время очевидно, что инфекция сама по себе не является непосредственной причиной комплек-са разнообразных метаболических, структурных и функциональных рас-стройств, свойственных сепсису. Очевидно, что сепсис представляет собой системный воспалительный ответ, индуцируемый не только комплексом ток-сических соединений, присущих бактериальной клетке, но и громадным ко-личеством образующихся медиаторов воспаления в клетках различных орга-нов и тканей, обладающих взаимопотенцирующим действием и обусловли-вающим полиморфизм клинических проявлений патологии.
Характерным признаком сепсиса является развитие лихорадочной реак-ции, обусловленной избыточной продукцией эндопирогенов. В ряде случаев у пожилых субъектов с исходно нарушенной терморегуляцией сепсис разви-вается на фоне гипотермии.
Нарушения внешнего дыхания проявляются вначале развитием гипервен-тиляционного ответа с последующим формированием дыхательного алкалоза и утомлением дыхательной мускулатуры.
Выраженные функциональные сдвиги свойственны сердечно-сосу-дистой системе, которые в конечном итоге в значительной мере определяют исход сепсиса, причем в ранней фазе сепсиса отмечается снижение периферическо-го сосудистого сопротивления на фоне увеличения сердечного выброса, ре-зультатом чего является гипотензия. Позднее сердечный выброс может сни-жаться, между тем периферическое сосудистое сопротивление либо остается сниженным, либо возрастает, однако гипотензия сохраняется.
Естественно, что снижение артериального давления, а также патогенное воздействие токсических и ферментных факторов патогенности микроорга-низмов являются причинами развития преренальной, а затем ренальной фор-мы почечной недостаточности с характерными признаками ее в виде гипера-зотемии и олигурии.
Достаточно быстро вовлекается в системный воспалительный процесс пе-чень, развиваются желтуха, диспротеинемия.
При сепсисе нередко поражается и центральная нервная система, что про-является дезориентацией больного, летаргией, вобуждением.
Одним из ранних проявлений сепсиса является расстройство коагуляци-онного гемостаза и фибринолиза, развитие ДВС-синдрома.
Неуклонное падение артериального давления, депонирование крови в пе-риферических сосудах, развитие явлений стаза, внутриорганных и внутрипо-лостных геморрагий являются важнейшими факторами прогрессирующей острой сосудистой недостаточности, полиорганной недостаточности, пер-вичной остановки дыхания и гибели больного.
Грозным осложнением сепсиса является септический шок, характери-зующийся прогрессирующей гипотензией, несмотря на инфузионную тера-пию, нарушением тканевой перфузии, развитием лактатацидоза, олигурии, полиорганной недостаточности, расстройствами гемостаза и микроциркуля-ции, развитием геморрагического синдрома.
Септический шок скоротечен, диагностика его достаточно трудна, не-смотря на стереотипность клинических проявлений, требует незамедлитель-ной патогенетически обоснованной терапии, адаптированной к характеру ме-таболических и функциональных расстройств у конкретного данного больно-го.
Какова же динамика образования воспалительных медиаторов, опосре-дующих цитопатогенные эффекты токсических факторов грамположитель-ной и грамотрицательной микрофлоры в процессе развития сепсиса и септи-ческого шока?
В настоящее время более четко систематизированы механизмы развития эндотоксикоза и соответственно грамотрицательного сепсиса.
Первичные или начальные этапы развития обусловлены способностью эн-дотоксина рецептироваться различными клетками крови, в частности, тром-боцитами, макрофагами, эндотелиальными клетками, нейтрофилами, базо-филами, эозинофилами, тучными клетками, гепатоцитами.
Активная клеточная акцепция ЛПС в организме объясняет феномен дис-социации между степенью эндотоксемии и тяжестью клинических проявле-ний патологии, когда при отсутствии циркулирующего токсина в крови раз-вивается характерная картина токсикоза и шока.
Важнейшими медиаторами септического воспалительного ответа являют-ся комплемент; продукты метаболизма арахидоновой кислоты – лейкотрие-ны, простагландины, простациклин, тромбоксан; цитокины – ФНО, ИЛ-1, ИЛ-6, ИЛ-8; гистамин; клеточные адгезивные молекулы; каскад ферментов прокоагулянтной, антикоагулянтной и фибринолитической систем; лизосо-мальные ферменты; активные формы кислорода; оксид азота и др. (Dinarello C.A., Clowes G.H.A., Gordon A.H. et al., 1986; Evans G.F., Snyder V.M., Butler L.G., 1989; Jоbotson G.C., Wallace J.L., 1989).
Указанные медиаторы, что очевидно, являются и медиаторами локальной воспалительной реакции. Детальная классификация этих медиаторов, их происхождение и оценка биологического действия даны выше.
На раннем этапе эндотоксемии мононуклеары служат источником выбро-са ФНО и ИЛ-1, являющихся основными медиаторами эндотоксе-мии. Отме-чено также и возрастание ИЛ-6. Антигенстимулированные макро-фаги спо-собствуют образованию метаболитов арахидоновой кислоты — лейкотриенов, простагландинов, тромбоксана А2, протеолитических ферментов, активных форм кислорода, ФАТ, оксида азота (Зербина Д.Д., Лукасевич Л.Л., 1989).
Антигенстимулированные полиморфноядерные лейкоциты при септиче-ских реакциях также являются источником образования ряда цитокинов, в частности, ФАТ, фактора хемотаксиса эозинофилов (ФХЭ), катионных бел-ков, нейтральных и кислых протеаз, эндопирогенов, лейкотриенов, простаг-ландинов, свободных радикалов.
В процессе дегрануляции тучных клеток и базофилов у больных с систем-ным воспалительным процессом высвобождаются гистамин, серотонин, ФХЭ, ФХН, ФАТ, лейкотриены, протеазы.
Возникающие при септических состояниях реакции адгезии и агрегации тромбоцитов также приводят к высвобождению комплекса биологически ак-тивных соединений, в частности, катехоламинов, серотонина, тромбоксана А2, тромбоцитарных факторов свертывания крови.
Каскад комплемента, как и множество других реакций, вовлечен в пато-физиологию сепсиса. Патологическая активация комплемента может начи-наться при участии бактерий, иммунных комплексов, поврежденных клеток эндотелия (Harlan J., Winn R., Hildebranolt S., Harker L., 1983). В свою оче-редь, продукты каскада комплемента могут активировать нейтрофилы, мак-рофаги, тромбоциты, которые включаются в системную воспалительную ре-акцию с помощью лизосомальных энзимов, цитокинов, свободных радика-лов, продуктов метаболизма арахидоновой кислоты.
Клинические наблюдения показывают, что при сепсисе раньше всего по-ражаются легкие. Основная причина дисфункции легких обусловлена повре-ждением эндотелия под влиянием эндотоксина и цитокинов: ФНО, ИЛ-1, ФАТ лейкотриенов, тромбоксана А2, оксида азота, свободных радикалов, вы-зывающих повышение проницаемости сосудов. Однако избыточное накопле-ние вазоактивных соединений при септическом шоке сочетается с неодно-значным изменением тонуса сосудов: вазодила-тирующий эффект нередко сочетается с вазоконстрикцией и развитием локальной ишемии. Последнее связано, по-видимому, с нарушением сбалансированности прессорных и де-прессорных факторов в сосудах различных органов и тканях. В качестве примера можно привести следующие нарушения взаимодействия вазоактив-ных соединений в динамике сепсиса.
Так, установлено, что эндотоксин, ФНО, ИЛ-1 активируют NO-син-тетазу в гладкомышечных клетках эндотелия сосудов и приводят к биосинтезу и ос-вобождению значительного количества NO (Forstermann H., Schmidt H.H., Pollock J.C., 1991; Марков Х.М., 1996) В свою очередь, NO внутри гладко-мышечной клетки связывается с геминовой простетической группой цито-зольной гуанилатциклазы, образуя нитрозилгеминовый комплекс, являю-щийся активатором гуанилатциклазы. Последняя обеспечивает возрастание уровня цГМФ в гладкомышечных элементах и развитие вазодилятации сосу-дов при септических состояниях. Важным внутриклеточным фактором акти-вации сосудистой NO-синтетазы является кальций, который в комплексе с белком кальмодулином переводит фермент в активное состояние (Раевский К.С., 1997).
Таким образом, опосредованно через образование NO при септических состояниях могут возникать вазодилатация, снижение чувствиительности гладкомышечных элементов сосудов к действию прессорных факторов.
Однако в ряде работ показано, что в процессе развития септического со-стояния возможно возрастание уровня тромбоксана А2, серотонина, катехо-ламинов, что может привести к развитию сосудистых спастических реакций.
Обращает на себя внимание и тот факт, что ФНО и ИЛ-1 свойственна прямая цитотоксичность, реализуемая через экспрессию соответствующих генов с последующим развитием апоптоза (программированной гибели кле-ток). Экспериментально установлено, что ФАТ ФНО вызывают развитие ги-потонии, повышение проницаемости резистивных сосудов с экстравазацией воды, альбумина, эритроцитов.
Результаты многочисленных исследований свидетельствуют о важной ро-ли свободных радикалов в дезинтеграции биологических мембран клеток и сосудистой стенки при сепсисе и септическом шоке.
Проведенные нами исследования в экспериментах с моделированием хо-лерного эндотоксикоза в опытах на белых крысах позволили установить до-зозависимую активацию процессов липопероксидации, характеризующуюся избыточным накоплением в плазме крови и эритроцитах малонового диаль-дегида, диеновых конъюгатов на фоне подавления активности СОД и катала-зы — ключевых ферментов антиоксидантной системы (Понукалина Е.В., Ки-ричук В.Ф., Чеснокова Н.П., Адамов А.К., 1997; Понукалина Е.В., Чеснокова Н.П., Афанасьева Г.А., 1998; Понукалина Е.В., Киричук В.Ф., 1998).
Параллельно проведенное изучение реологических свойств крови на мо-дели холерного эндотоксикоза, достигаемого внутрибрюшинным введением белым крысам эндотоксина в дозе, эквивалентной ДЛ50, свидетельствовало об усилении разрушения эритроцитарных агрегатов, нарушении деформи-руемости эритроцитов, появлении так называемых «жестких» эритроцитов. Как известно, появление «жестких» эритроцитов в значительной мере может быть обусловлено активацией процессов липопероксидации, приводящей к распаду лецитина и усилению гемолиза.
Касаясь значимости активации процессов свободнорадикального окисле-ния в динамике эндотоксикоза, следует отметить, что промежуточные про-дукты пероксидации липидов обладают мощным сосудорасширяющим дей-ствием, а конечная генерация гипохлоридных и гипероксидных радикалов полностью дезорганизует метаболизм клеток.
Резюмируя вышеизложенное, следует заключить, что коллаптоидно-шоковую артериальную гипотонию при сепсисе обусловливают вазоактив-ные соединения с разнонаправленными механизмами действия: ФНО, ФАТ, ИЛ-1, лейкотриены, простагландины, кинины, комплемент, гистамин, серо-тонин и др. Молекулярно-клеточные механизмы их действия представлены выше.
Прогрессирующая гипотония в динамике шока сочетается с экстра-вазацией жидкости, патологическим депонированием крови, развитием стаза, тромбоза, геморрагий в сосудах микроциркуляторного русла различных пе-риферических органов и тканей, что приводит к развитию в них дистрофиче-ских процессов, очаговых некрозов.
Расстройства микроциркуляции при септических состояниях обусловлены активацией трех взаимосвязанных механизмов:
а) внутреннего механизма формирования протромбиназы за счет актива-ции XII фактора с участием комплемента, иммунных комплексов, высоко-молекулярного кининогена;
б) внешнего механизма гемостаза за счет освобождения эндотелием, гра-нулоцитарно-макрофагальными элементами тромбопластина;
в) тромбоцитарного звена системы гемостаза, так как тромбоциты первы-ми захватывают липополисахарид (эндотоксин), активируются и стимулиру-ют различные клеточные элементы к продукции цитокинов – ФАТ, ФНО, ИЛ-1, протеаз, усиливающих и ускоряющих коагуляцию крови.
Следует отметить, что повышенную свертываемость крови можно диагно-стировать лишь в начальной стадии эндотоксикоза, а в поздней — и тем более при шоке – система гемостаза находится в состоянии выраженной гипокоа-гуляции вплоть до полного несвертывания крови. Это обстоятельство объяс-няется мощным усилением антикоагуляционного потенциала крови.
Механизмы гипокоагуляции крови включают в себя прямое влияние эндо-токсина на антикоагулянтные механизмы за счет усиления высвобождения антикоагулянтов клеточно-тканевого происхождения. В ответ на первичное усиление активности прокоагулянтной системы крови под влиянием эндо-токсина и цитокинов возникает компенсаторное усиление синтеза и секреции естественных первичных антикоагулянтов, в частности, гепарина, антитром-бина III -I-антитрипсина, антитромбопластина, 2-макроглобулина и др. В то же время в динамике эндотоксикоза в кровотоке появляются вторичные антикоагулянты, образующиеся в ходе ферментативной деактивации и дегра-дации коагуляционных факторов, а также фибринолиза. Эти вторичные анти-коагулянты представлены фибрином, продуктами деградации фибрина и фибриногена, клеточными протеиназами, расщепляющими активные факто-ры коагуляции, неферментативными комплексами адреналина с гепарином, фибриногеном и его фрагментами.
Характерной для эндотоксикоза является и активация фибринолиза по внутреннему и внешнему механизмам (Грачев С.В., Якунин Г.А., Новочадов В.В., Ярошенко И.Ф., 1992).
Первый связан с активацией XII фактора, который запускает не только каскад последовательно активирующихся коагуляционных факторов, но од-новременно растормаживает плазменные активаторы плазминогена, увели-чивая содержание и активность плазмина.
Активация внешнего механизма фибринолиза обеспечивается эндо-токсином за счет секреции многочисленных протеаз активированными клет-ками иммунной и ретикулоэндотелиальной системы.
В ряде исследований отмечено, что при эндотоксиновом шоке система фибринолиза может не усиливаться, а угнетаться. Это может быть обуслов-лено чрезмерной активацией антикоагуляционных механизмов, обеспечи-вающих помимо блокады прокоагулянтных факторов ингибирование систе-мы фибринолиза.
Важнейшими факторами антифибринолитической системы являются бел-ки острой фазы с ингибиторной функцией по отношению к широкому спек-тру протеаз, в том числе и плазмину. Индукторами синтеза белков острой фа-зы являются ИЛ-1, ИЛ-6, ФАТ, ФНО, -интерферон, ростовые факторы кле-ток. Антифибринолитическим действием обладают многие липиды плазмы крови – холестерин, ЛПОНП, ЛПНП, триглицериды.
Обращает на себя внимание тот факт, что большинство экспери-ментальных исследований по изучению влияния бактериальных эндотокси-нов на состояние процессов коагуляционного гемостаза и фибринолиза про-ведено на высокочувствительных животных – морских свинках, кроликах, белых мышах, для которых характерна чрезвычайно короткая фаза гиперкоа-гуляции в динамике ДВС-синдрома, сменяющаяся гипокоагуляционными сдвигами с выраженным истощением факторов прокоагулянтной системы на фоне активации антикоагулянтных механизмов.
Следует отметить, что изучение молекулярно-клеточных механизмов рас-стройств гемостатического потенциала крови наиболее целесообразно в экс-перименте в начальном периоде индукции гиперкоагуляционных сдвигов для выявления всей динамики расстройств взаимодействия прокоагулянтной, ан-тикоагулянтной и фибринолитической систем для разработки принципов ме-дикаментозной коррекции, обеспечивающей профилактику гипокоагуляци-онных сдвигов, свойственных эндотокси-новому шоку.
Последнее определило необходимость изучения комплекса показателей прокоагулянтной, антикоагулянтной и фибринолитической систем в динами-ке интоксикации, индуцируемой введением холерного эндотоксина в субле-тальных и частично летальных дозах белым крысам, обладающим достаточно высокой резистентностью к действию указанного патогенного фактора.
Использование нескольких модификаций экспериментов с подкожным и внутрибрюшинным введением эндотоксина позволило установить некоторые особенности инициирующих механизмов расстройств гемостатического по-тенциала крови. При легких формах бактериальной интоксикации активация антикоагулянтных механизмов и системы фибринолиза может предшество-вать активации прокоагулянтной системы (Kirichuk V.F., Chesnorova N.P., Ponucalina E.V. et al., 1995; Понукалина Е.В., Киричук В.Ф., Чеснокова Н.П., Белов Л.Г., 1995).
В условиях комплексного введения холерного энтеро- и эндотоксина бе-лым крысам в сублетальных дозах, а также частичнолетальных, несмотря на их резистентность к воздействию энтеротоксина и отсутствие развития диа-реи и дегидратационного синдрома, возникала определенная модификация эффектов на изучаемые показатели активности про-коагулянтной, антикоагу-лянтной и фибринолитической систем по сравнению с таковыми показателя-ми в аналогичные сроки наблюдения в группе животных, которым вводили лишь холерный эндотоксин.
Так, в условиях комплексного воздействия токсинов спустя 4 часа после их введения отмечались укорочение силиконового времени свертывания кро-ви, снижение ИДКА, (индекса диапазона контактной активации), что свиде-тельствовало о внутрисосудистой активации плазменных факторов сверты-вания крови. Между тем введение одного холерного эндотоксина не отража-лось на состоянии активности прокоагулянтной системы крови в указанные сроки интоксикации. Комплексное введение эндо- и энтеротоксинов приво-дило к увеличению уровня антитромбина III, суммарной фибринолитической активности крови, снижению содержания фибриногена, как в соответствую-щий период интоксикации индуцированной лишь введением эндотоксина (Ponucalina E., Kirichuk V., Chesnokova N., Belov L., 1997). При этом уровень активаторов плазминогена заметно возрастал как по сравнению с контролем, так и по сравнению с показателями у животных, которым вводили лишь эн-дотоксин.
Спустя сутки после введения холерного эндотоксина в сублетальной дозе обнаруживалось укорочение спонтанного времени свертывания крови, уро-вень антитромбина III оставался высоким, суммарная фибринолитическая и плазминовая активность крови превышала контрольные показатели, как и на предыдущей стадии интоксикации, одновременно возрастали активность ак-тиваторов плазминогена и антиплазминовая активность крови.
В другой модификации экспериментов спустя сутки после комплексного воздействия холерных эндо- и энтеротоксинов отмечалось увеличение не только спонтанного, но и силиконового времени свертывания крови. Однако показатели антикоагулянтной активности крови и системы фибринолиза бы-ли значительно выше показателей нормы, как и в группе животных с введе-нием лишь одного эндотоксина.
Таким образом, в используемых нами дозировках (100 мкг/кг или ДЛ 50 для мышей) холерный энтеротоксин не оказывал модифицирующего воздей-ствия на эффекты эндотоксина, на антикоагулянтные механизмы и систему фибринолиза белых крыс, отличающихся устойчивостью к цитопатогенному воздействию экзотоксина на энтероциты.
Увеличение дозы воздействия эндотоксина и энтеротоксина до развития частичнолетального эффекта сочеталось с развитием гиперкоагуляцион-ных сдвигов спустя 4 часа после введения токсинов. При этом активность анти-тромбина III, суммарная фибринолитическая активность, плазминовая актив-ность, активность активаторов плазминогена достаточно превышали кон-трольные показатели. В то же время возрастание дозы воздействия токсинов сопровождалось снижением содержания фибриногена и антитромбиновой активности крови по сравнению с показателями контрольной группы.
Резюмируя вышеизложенное в целом, следует заключить, что характер-ной особенностью инициации расстройств гемостаза при легких сублеталь-ных или частичнолетальных формах интоксикации, индуцирован-ной введе-нием только холерного эндотоксина или сочетанным воздействием эндо- и энтеротоксина, является активация антикоагулянтных механизмов и системы фибринолиза, сочетающаяся с гиперкоагуляционными сдвигами или опере-жающая их развитие.
Результаты проведенных нами экспериментов позволили выявить важную закономерность: высокая резистентность белых крыс к воз-действию холер-ных эндо- и энтеротоксинов сочетается с развитием длительной фазы гипер-коагуляции, несмотря на выраженную активацию антикоагулянтных меха-низмов и системы фибринолиза. Используемые нами варианты моделирова-ния холерной интоксикации на высокорезистентных животных позволяют не только уточнить нарушение взаимодействия прокоагулянтной, антикоагу-лянтной и фибринолитической систем в начальные периоды легкой формы интоксикации, но и открывают возможности для разработки патогенетически обоснованных принципов медикаментозной коррекции коагуляционного ге-мостаза на начальной фазе тромбогеморрагического синдрома, осложняюще-го различные формы септической грамотрицательной инфекции.
Как свидетельствуют данные литературы, ведущий механизм активации коагуляционного гемостаза при эндотоксикозе связан с тромбоцитарной и тромбопластиновой активацией его под влиянием комплемента, цитокинов (ФАТ, ФНО, ИЛ-1, ИЛ-3, тромбоксан А2). Преобладающими поставщиками тромбопластина являются эндотелий и макрофагально-гранулоцитар-ные клетки. При этом в органах не развивается тромботический процесс, несмот-ря на выраженную его активацию. В условиях гипоксии и ацидоза происхо-дят микроагрегация тромбоцитов и нейтрофилов, адгезированных на эндоте-лиоцитах, а также выпадение волокон нестабилизированного фибрина в виде микроочагового или сетчатого тонкопленчатого покрытия стенки сосудов. Взвешенные в плазме крови тромбоцитарно-эритроцитарные микроагрегаты сцементированы растворимым фибрином. Данные изучения коагуляционного потенциала крови свидетельствуют о том, что в динамике эндотоксикоза и эндотоксинового шока происходит блокада стабилизации фибрина за счет возрастания антипротеазного потенциала крови в связи с усилением макро-фагально-гранулоцитарной продукции цитокинов, усилением синтеза пече-нью белков острой фазы, обладающих антикоагулянтной активностью.
Активируемая в условиях эндотоксикоза NO-синтетаза эндотелия обеспе-чивает избыточную продукцию NO, обладающего не только выраженным ва-зодилатирующим действием, но и выступающим в роли ингибитора агрега-ции тромбоцитов и тем самым подавляющим процессы тромбообразования.
Результаты проведенных нами экспериментов на модели холерной инток-сикации, достигаемой введением возрастающих доз эндотоксина от субле-тальных до частичнолетальных доз (ДЛ25) убедительно свидетельствовали о доминирующем преобладании активации в динамике интоксикации системы фибринолиза, на что указывало выраженное возрастание суммарной фибри-нолитической активности крови, плазминовой активности крови, активности активаторов плазминогена (Понукалина Е.В., Киричук В.Ф., 1998; Понука-лина Е.В., Киричук В.Ф., Чеснокова Н.П., Белов Л.Г., 1997).
В двух модификациях экспериментов с подкожным введением холерного эндотоксина в сублетальной дозе и внутрибрюшинным сочетанным введени-ем эндо- и энтеротоксина в частично смертельной дозе удалось зарегистри-ровать одновременное с активацией системы фибринолиза возрастание уров-ня фибриногена, являющегося одним из белков острой фазы.
В необратимой стадии эндотоксикоза иногда возможно усиление генера-лизованной диссеминации свертывания крови в магистральных сосудах в связи с исчерпанием антикоагуляционных механизмов гемостаза.
Полисистемность и полифункциональность действия эндотоксина в орга-низме людей, опосредованные комплексом цитокинов, являющихся в значи-тельной мере и медиаторами воспаления, обусловливает выражен-ные рас-стройства микроциркуляции, регионарного кровотока и системной гемоди-намики с последующим развитием синдрома полиорганной недостаточности.
Для септического шока характерны определенные особенности и общие закономерности нарушения структуры и функции в тех или иных органах и тканях.
предыдущий раздел | содержание| следующий раздел
Значение для медицины
Разработанный Грамом этиологический тест оказался востребованным не только в микробиологии. Информация, полученная благодаря ему, также продвинула на новый уровень медицину, в особенности лечение пациентов, зараженных грамотрицательными бактериями. Несмотря на то, что gram-negative bacteria (грамнегативные палочки) врачи причисляют к условно-патогенной микрофлоре, ошибочно считать их безобидными. Они вызывают бурную ответную реакцию организма и обладают высокой резистентностью, что часто приводит к летальным исходам.
У больных отмечается воспаление бронхолегочной системы в тяжелой степени. Вызывает его ЛПС, или липополисахаридный слой бактерий, которого лишены грамположительные микроорганизмы. Микробиология определяет этот компонент мембраны клетки как эндотоксин для человеческого организма, независимо от формы бактерии: спириллы или палочки. Попадая внутрь, он активизирует синтез цитокинов и иммунный ответ.
В итоге начинает развиваться локализованное воспаление. С течением времени токсины поступают в кровеносное русло и далее разносятся транспортной системой по всему телу. Больной начинает испытывать все более нарастающие признаки интоксикации. Растет частота дыхания и температура тела, кровяное давление падает. Проявляется токсический шок, который в некупированном состоянии заканчивается смертью.
Благодаря открытию Грама врачи смогли найти альтернативу малоэффективным в подобных случаях пенициллину и лизоциму. Например, объединение последнего с этилендиаминтетрауксусной кислотой, или EDTA. Помогли и успешные клинические испытания ампициллина, стрептомицина, хлорамфеникола и налидиксовой кислоты в борьбе с грамотрицательными бактериями.
Грамположительный мир
Эти микроорганизмы окрашиваются способом Грама в фиолетовый цвет. Смысл процедуры состоит в том, что толщина защитного слоя бактериальной клетки довольно высока, за счет чего краситель удерживается. Грамположительные бактерии представлены стафилококками, стрептококками. Кроме того, грамположительные бактерии – возбудители таких опасных недугов, как газовая гангрена, столбнячная инфекция, сибирская язва. От грамотрицательных бактерий они отличаются по строению и толщине клеточной стенки. Именно она определяет внешний вид микроорганизмов: спиралевидный холерный вибрион, шаровидная кокковая форма. Бактериальная клетка отличается от клеток млекопитающих наличием жесткого защитного каркаса, состоящего из плотного биополимерного слоя, и химическим составом. Этим обусловлена реакция бактерий на действие антибиотиков.
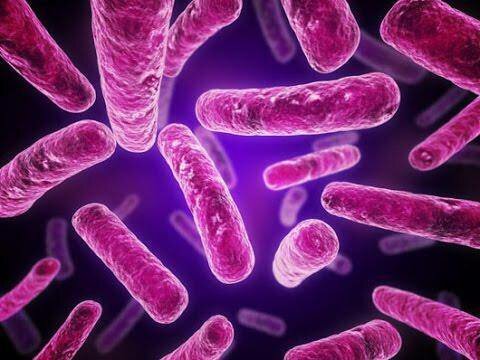
Грамположительные бактерии имеют толстый ригидный слой (клеточную стенку). Защитная оболочка состоит из полипептидов и полисахаридов. До 70% стенки составляет муреиновый мешок. В его состав входят: лизин, ацетилглюкозаминин, ацетилмурамовая кислота, диаминопимелиновая и тейхоевые кислоты.
Грам (+) и Грам (-) представители и их воздействие на организм
Итак, клеточная стенка грамположительных бактерий имеет лишь один слой. Единственное исключение, известное в современной микробиологии, – Deinococcus-Thermus. Несмотря на наличие защитной мембраны, при проведении теста она хорошо окрашивается в синий цвет.
Основными представителями Грам (+) бактерий являются:
- Кокковые или шаровидные (кроме протеобактерий Neisseria):
-
стафилококк, провоцирующий сепсис крови и гнойные высыпания на коже;
- стрептококк, ведущий к развитию ревматизма и тонзиллитов;
- Палочковидные:
-
фирмикуты, служащие источником сибирской язвы и токсических инфекций;
- клостридии, как возбудители столбняка и ботулизма;
- листерия, заражение которой приводит к воспалению мозга.
- Булавовидные:
-
коринебактерии, вызывающие дифтерию.
Грамотрицательные бактерии, более устойчивые к антителам за счет дополнительной мембраны, представлены такими разновидностями:
- Спиралевидные:
-
спирохеты, которые являются возбудителями лептоспироза, возвратного тифа и сифилиса;
- спириллы, вызывающие содоку – лихорадкоподобное состояние.
- Палочки:
-
риккетсии, чей главной характеристикой служит внутриклеточный паразитизм;
- хламидии – без лечения могут развиться ЗППП, конъюнктивит, пневмония.

Бактериальная трансформация
Преобразование является одним из трех способов горизонтального переноса генов , в которых экзогенный генетический материал проходит от бактерии к другому, а два другим , являющейся конъюгации (перенос генетического материала между двумя бактериальными клетками в непосредственном контакте) и трансдукции (введение чужеродной ДНК с помощью бактериофага вирус в бактерии — хозяина). В трансформации, генетический материал проходит через промежуточную среду, а поглощение полностью зависит от бактерии — реципиента.
В 2014 было известно , чтобы иметь возможность трансформации, примерно поровну разделены между около 80 видов бактерий , грамположительных и грамотрицательных бактерий; число может быть завышение , так как некоторые из отчетов поддерживается отдельными бумагами. Трансформация изучена с медицинской точки зрения важных видов грамотрицательных бактерий , таких как Helicobacter Pylori
,
легионелл
,
менингококк
,
гонококков
,
гемофильной
и
холерного вибриона
. Кроме того , было изучено в грамотрицательных видов , обитающих в почве , такие как
Pseudomonas stutzeri
,
Acinetobacter baylyi
и грамотрицательных патогенов растений , таких как
Ralstonia solanacearum
и
Xylella fastidiosa
.
Что такое грамотрицательные бактерии
Бактерии, которые не сохраняют кристаллическое фиолетовое пятно во время окрашивания по Граму, называются грамотрицательными бактериями. Слой пептидогликана, который отвечает за сохранение окраски кристаллического фиолетового, является тонким у грамотрицательных бактерий, и он зажат между внутренней цитоплазматической мембраной и внешней мембраной бактерий. Следовательно, грамотрицательные бактерии могут быть окрашены встречным окрашиванием сафранином во время техники окрашивания по Граму, давая цвет от красного до розового. кишечная палочка является грамотрицательным и используется в качестве модельного организма в большинстве исследований бактерий. Грамотрицательные бактерии являются более патогенными из-за их меньшей восприимчивости к антибиотикам. Устойчивость к антибиотикам грамотрицательных бактерий определяется внешней мембраной этих бактерий. Neisseria gonorrhoeae, Pseudomonas aeruginosa а также Иерсиния пестис как грамотрицательные бактерии являются патогенными.
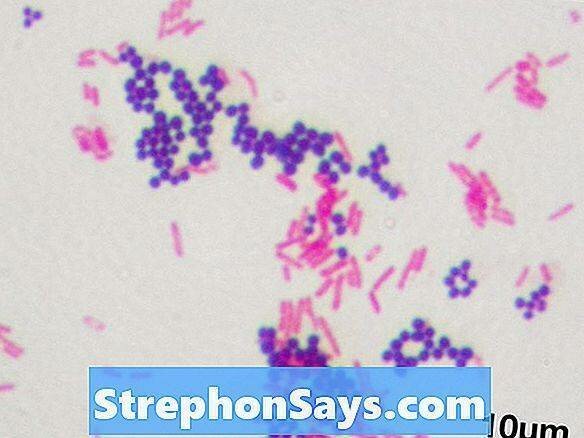
Рисунок 3: Грамотрицательные кокки и грамположительные палочковидные бактерии при окрашивании по Граму
Структура клеточной стенки и клеточной оболочки грамотрицательных бактерий
Клеточная стенка грамотрицательных бактерий имеет толщину 5-10 нм и содержит монослой пептидогликана. Основа пептидогликана частично сшита у грамотрицательных бактерий. Тейхоевая кислота не обнаружена в клеточной стенке грамотрицательных бактерий. Грамотрицательные бактерии состоят из клеточной оболочки снаружи клеточной стенки, называемой наружной мембраной, толщиной 7,5-10 нм. В наружной мембране грамотрицательных бактерий обнаружены липополисахариды, которые служат эндотоксинами. Наружная мембрана нековалентно заякорена в липопротеины, называемые липопротеинами Брауна, которые ковалентно связаны со слоем пептидогликана. Внутренняя и внешняя мембрана прилипают друг к другу сотнями бейеровских пятен.
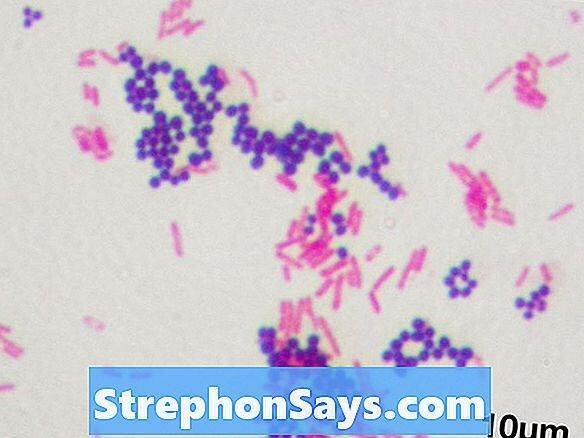
Рисунок 4: Грамотрицательная клеточная стенка
Нормы чистоты: 4 степени
| Степень | Состав мазка | Значение |
| 1 | Палочки Дедерлейна (лактобациллы) – большинство;Другие бактерии – единичные;Слизь – незначительно;Лейкоциты – до 10;Клетки эпителия – 5-10;Среда — кислая | Идеальный, но очень редкий вариант, который почти не встречается у женщин фертильного возраста, живущих половой жизнью |
| 2 | Палочки Дедерлейна – в большинстве;Грамположительные кокки – незначительно;Слизь – незначительно;Клетки эпителия – 5-10;Лейкоциты – до 10;Среда – слабокислая | Вариант нормы, характерный для большинства здоровых женщин |
| 3 | Грамотрицательная палочковая флора и кокки – большинство;Есть ключевые клетки;Палочки Дедерлейна – единичные;Слизь – умеренная;Лейкоциты – >10;Клетки эпителия – >10;Среда — нейтральная | Кольпит (вагинит) – воспаление слизистой влагалища. Возбудителем может быть хламидия, стафилококк, микоплазма, трихомонада, стафилококк, гемофильная палочка, а также сразу несколько инфекций |
| 4 | Палочки Дедерлейна – нет или единичные;Условно-патогенные и патогенные микроорганизмы – обильные;Слизь – много;Лейкоциты – >30;Клетки эпителия – много;Среда – нейтральная или щелочная, pH>4.5 | Интенсивное воспаление, которое сопровождается выраженной симптоматикой |
Совет, как правильно подготовиться к взятию мазка
Сдавать мазок на микрофлору следует не раньше чем спустя 3 дня после окончания менструации, так как клетки крови могут исказить результат. Идеальное время – 10-20 день цикла.
Для максимальной точности показателей рекомендуется соблюдать несколько правил:
- за две недели до анализа прекратить прием антибиотиков и антимикозных (противогрибковых) средств;
- за 2-3 дня исключить занятия сексом;
- за 2 суток прекратить использование любых вагинальных форм лекарств – суппозиториев, влагалищных таблеток, спреев, кремов, растворов;
- непосредственно перед процедурой исключить спринцевание и подмывание.
Биологический материал для исследования
Для лабораторной диагностики инфекционного заболевания пациент должен сдать один или несколько из нижеописанных анализов:
- Мазок мокроты для микроскопии. Забор производится ватными палочками или тампонами из носоглотки и не требует специальной подготовки.
- Анализ кала. Его расшифровка позволяет выявить след токсинов, которые вырабатывают грамположительные бактерии.
- Мазок из влагалища. Назначают для подсчета соотношения положительных и отрицательных микробов при вагинитах. Гигиенической подготовки не нужно.
- Пункции различных жидкостей: перинатальной, синовиальной, плевральной. Назначают в исключительных случаях и проводят только по указанию врача.
Метод определения «грамположительности» и «грамотрицательности»
При наличии признаков заражения организма врач назначает окрашивание по Граму. Это необходимо для определения типа инфекции: бактериальной, вирусной, грибковой или паразитарной, поскольку все виды лечатся по-разному.
Образец для исследования может быть в виде:
- мокроты, откашливаемой из лёгких;
- мочи, собранной в специальный контейнер;
- крови, сданной в лаборатории;
- слюны;
- мазков из влагалища;
- кала.
С помощью определенных методик определяется тип микроорганизмов в плевральной, перитонеальной жидкости.
Лаборант использует специальную технику окрашивания, чтобы легче увидеть клеточные организмы под микроскопом. Если результаты окрашивания по Граму отрицательные, это означает, что в образце не было обнаружено бактерий. Если положительные, значит, присутствовали микроорганизмы. Результаты также будут включать информацию о форме бактерий, по которой можно судить о типе инфекции.
Хотя результаты могут не идентифицировать точный тип бактерий, но они помогают врачу приблизиться к выяснению того, что вызывает заболевание и как лучше его лечить.
Результаты окрашивания по Граму также могут показать наличие грибковой инфекции (дрожжи или плесень).
При лечении болезней, вызванных грамположительными организмами, врачу необходимы следующие сведения:
- тип бактерий;
- устойчивость к противомикробным препаратам;
- образуют ли бактерии токсины.
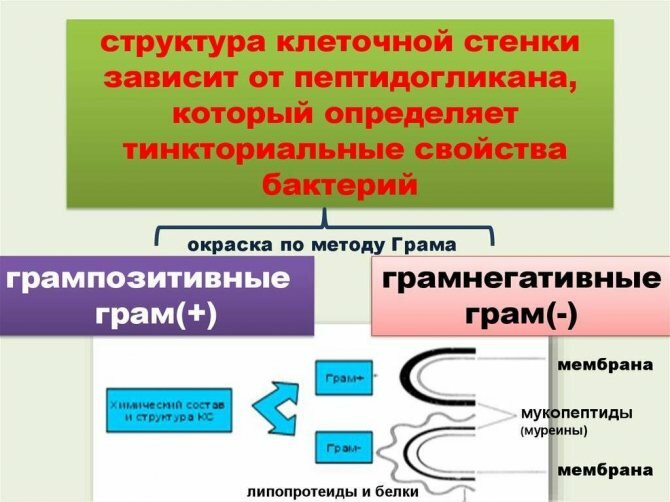
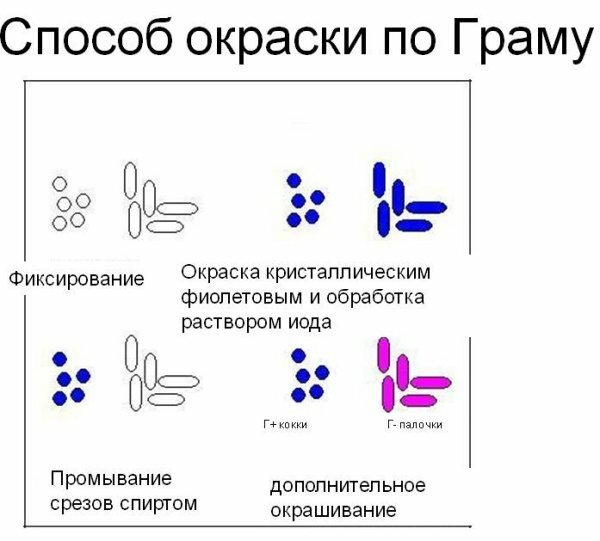
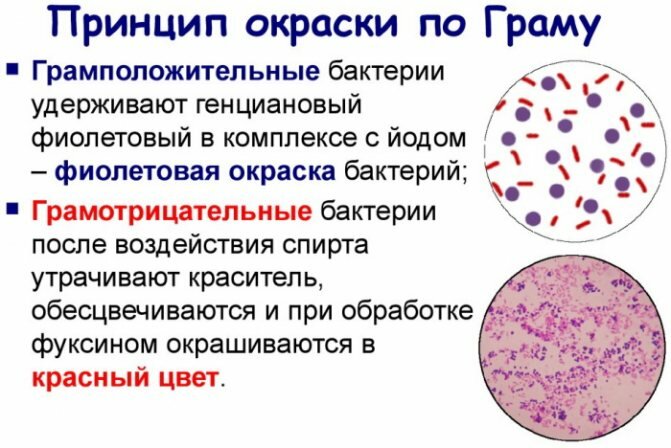
Сущность метода Грама
Основой метода Грама является принцип разделения бактерий на микроорганизмы со знаками «плюс» и «минус» по Граму, основываясь на разном химическом составе клеточных стенок микроорганизмов.
Для определения грамположительных и грамотрицательных бактерий препарат, нанесенный на стекло тонким равномерным слоем, вначале фиксируют с помощью нагревания над горелкой. Затем окрашивают анилиновым красителем – метиловым фиолетовым. После чего фиксируют йодом, дают подсохнуть и смывают при помощи спирта.
- Грамположительные (Грам +) виды приобретают ярко-синюю окраску.
- Грамотрицательные (Грам –) бактерии обесцвечиваются.
Заключающим этапом является окрашивание препарата контрастным красителем красного цвета, который позволяет получить грамотрицательные микроорганизмы красного или розового цвета. Это обусловлено тем, что краситель не может проникнуть в клетку из-за толстого ее внешнего слоя, окрашивая только поверхность.
Окрашивание по Граму. Кокки (шаровидные) — грамположительные и бациллы (палочки) — грамотрицательные
Мертвые микробы приобретают более яркую окраску, по сравнению с живыми.
Дисбаланс
Грамположительные и грамотрицательные бактерии обитают практически во всех частях человеческого тела, на коже, в кишечнике, во рту и носу. Иногда они вызывают болезни, но в большинстве случаев микроорганизмы живут в гармонии со своими хозяевами, обеспечивая жизненно важные функции, необходимые для выживания человека.
Причины, по которым нарушается баланс:
- Плохая диета и неправильный выбор продуктов.
- Чрезмерное использование антибиотиков.
- Недостаток сна.
- Эмоциональный стресс.
Перенаселение одного вида бактерий приводит к инфекциям и другим проблемам со здоровьем. При уменьшении хороших микроорганизмов в кишечнике защитный барьер понижается, что позволяет проникать в организм вредным бактериям, токсинам и большим молекулам белка.
Что происходит, когда плохие бактерии чрезмерно колонизируются:
- Увеличивается проницаемость кишечника.
- Плохие бактерии распространяются в мочевыводящую систему, вызывая инфекцию мочевыводящих путей.
- Повышается утомляемость из-за перегрузки токсинами.
- Снижается активность иммунной системы, что способствует развитию аллергии и заболеваний, связанных с аутоиммунной реакцией, таких как болезнь Крона, язвенный колит, ревматоидный артрит, кожная инфекция и инфекция влагалищного тракта.
- Развивается диарея из-за кишечной реакции на вредные бактерии.
Бактерии присутствуют и в здоровых легких. Когда хрупкий баланс популяций бактерий в легких нарушается, это может привести к развитию таких заболеваний, как астма и хроническая обструктивная болезнь легких.
Основное внимание следует обратить на последствия нарушения микробного баланса в пищеварительной системе. Оно может иметь негативные последствия не только для органов ЖКТ, но и нервной, метаболической и иммунологической системы.
Поэтому сохранение баланса в вечной битве между «хорошими» и «плохими» бактериями как среди грамположительных, так и грамотрицательных микробов — это путь к здоровью и хорошему самочувствию.
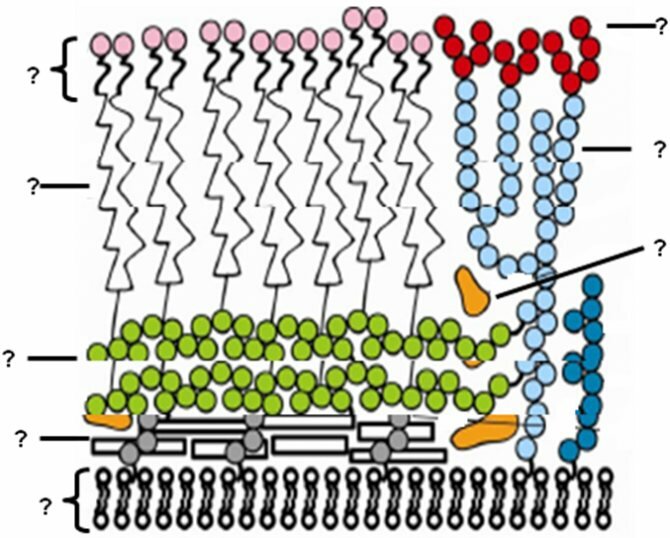
Строение клеточной стенки
Оболочка любой бактерии состоит из специального вещества – муреина. Его молекула представляет собой цепи полисахаридов, расположенных параллельно. Полисахариды, в свою очередь, связаны между собой цепями аминокислот, расположенных перекрестно.
Данная связь обуславливает крепкость, упругость оболочки, ее способность держать форму. Своеобразная плетеная сетка является защитой внутреннего слоя микроорганизма от действия разрушающих факторов, препятствует попаданию внутрь воды. При этом просветы между цепочками позволяют клетке поглощать питательные вещества, словно поры.
У отрицательных видов строение клеточной оболочки значительно сложнее, что позволяет ей быть защищенной от действия таких сред, как слюна, желудочный сок, другие жидкости с содержащимся в них лизоцимом – ферментом, обладающим антибактериальными свойствами. Снаружи более тонкая оболочка окружена пленкой из липидов и полисахаридов – гладким поверхностным слоем.
Суть метода
В микробиологии этот метод приравнивается к сложным. На бактерии действуют основным и дополнительным красителями, а также обесцвечивающим веществом. Наглядно весь процесс окрашивания можно представить следующими шагами:
- Предметное стекло очищают от жира и покрывают тонким слоем собранного мазка, после чего высушивают его естественным путем.
- Фиксируют физическим или химическим способом, вызывая коагуляцию белков.
- Через фильтр-бумагу наносят первый краситель и оставляют в покое на пару минут.
- После чего убирают пигмент, добавляют на стекло раствор Люголя и выдерживают одну минуту.
- Удаляют йодистый раствор, а бактерии промывают этиловым спиртом до обесцвечивания.
- Ополаскивают стекло дистиллированной водой около минуты.
- Наносят на стекло второй краситель и оставляют его не более чем на 5 минут.
- Снова ополаскивают и высушивают фильтр-бумагой.
Открытие Ганса Христиана Грама
В отличие от своего почти полного тезки, Ганс Христиан Грам не писал сказок, однако сделал для человечества ничуть не меньше. Его называют одним из основателей микробиологии, ведь именно Грам в конце XIX века разработал метод разделения основных двух классов бактерий. Его метод окраски микроорганизмов позволил разделить все царство бактерий на две группы – грамположительные и грамотрицательные бактерии.
Особенности каждой из групп понятным языком можно описать так:
1. Грамположительные бактерииК ним относятся микроорганизмы, которые при помощи анилинового красителя окрашиваются в синий цвет. Такие бактерии в процессе жизнедеятельности образуют споры и выделяют экзотоксины. Оболочка грамположительных бактерий очень толстая, однако через нее легко проникают любые жидкости, в том числе и те, которые содержат антибиотик. Исходя из этого, уничтожить такие болезнетворные бактерии антибактериальными средствами гораздо легче, чем представителей другого вида.
2. Грамотрицательные бактерииВ эту группу входят микробы, которые после удаления анилинового красителя окрашиваются фуксином в красный цвет. В отличие от грамположительных бактерий, эти микроорганизмы не образуют спор, но выделяют эндотоксины, способные нанести вред организму.
Главным отличием грамотрицательных микробов являются наличие не одной, а сразу двух клеточных стенок, между которыми располагается периплазматическое пространство. Двойная «броня» серьезно увеличивает защитные свойства таких микроорганизмов, и пусть их клеточные стенки гораздо тоньше, сложное строение создает таким бактериям мощную защиту, справиться с которой сможет не каждый антибиотик. Благодаря своим защитным свойствам способность грамотрицательных бактерий противостоять лекарствам стала настоящей проблемой для клинической фармакологии, в частности, для разработчиков антибактериальных средств.
К тому же внешняя капсула грамотрицательных микробов (липополисахаридный слой), способна оказывать вредное воздействие на человеческий организм, так как именно этот наружный слой является источником эндотоксинов, вызывающих воспалительные процессы в организме и его интоксикацию.
Использование этих знаний при лечении болезней
При диагностике заболевания для определения более эффективного лечения обязательно применяется метод Грама для определения того, какие микроорганизмы вызвали болезнь: грамположительные или грамотрицательные бактерии. Антибиотики назначаются в зависимости от этого. Ведь неправильно выбранное лечение может только усугубить ситуацию.
Для определения возбудителя исследуется мокрота, выделения из носа или влагалища, анализ кала, синовиальной или плевральной жидкости. Эти образцы подвергаются обследованию по методу Грама.
Сложнее всего вылечить заболевания, вызываемые грамотрицательными бактериями. В основном на них воздействуют сочетанием двух антибиотиков или же препараты нового поколения. Эфективными против них могут быть «Ампициллин» или «Амоксициллин», «Хлорамфеникол», «Стрептомицин», а также группа цефалоспоринов. Они могут справиться с внешней мембраной таких бактерий.
Знания о строении стенки бактерий позволило улучшить эффективность лечения инфекционных заболеваний.
Метод Грама
Человек давно ищет пути лечения инфекционных заболеваний. После того как было обнаружено существование патогенных бактерий, ученые стараются их классифицировать, чтобы выяснить, как с ними бороться. Лучший способ был предложен в 1884 году врачом Гансом Кристианом Грамом. Он довольно простой, но информативный и используется до сих пор. По этому методу различаются грамположительные и грамотрицательные бактерии.
Доктор Грам использовал при изучении микроорганизмов фиолетовый краситель и заметил, что некоторые из них поддаются окрашиванию, другие же – нет. Он выяснил, что связано это с особенностями клеточных стенок бактерий
Так как эти микроорганизмы состоят из одной, реже двух клеток, для них очень важно иметь прочную оболочку. Поэтому клеточные стенки у них имеют сложное строение
Они защищают внутреннюю среду от проникновения жидкостей. Сложнее всего строение у грамотрицательных бактерий. Они устойчивы к проникновению слюны, желудочного сока и других жидкостей.
Суть метода Грама в том, что исследуемую среду обрабатывают анилиновым красителем, фиксируют йодом, а затем смывают спиртом. При этом грамотрицательные бактерии обесцвечиваются, а грамположительные приобретают синюю окраску. После повторной обработки красным красителем отрицательные виды могут окраситься в розовый цвет, причем погибшие микроорганизмы окрашиваются ярче.

Применение метода в медицине
Метод Грама по разделению микроорганизмов на грамположительные и грамотрицательные бактерии способствовал совершенствованию микробиологических исследований. Он помогает выявлять устойчивость патогенных видов к лекарственным препаратам, разрабатывать новые антибиотики для борьбы с ними. Ведь прочная клеточная стенка грамотрицательных бактерий делает их нечувствительными к обычным антибактериальным препаратам. А оболочка грамположительных микроорганизмов, хоть и очень толстая, но проницаема для жидкостей и антибиотиков.
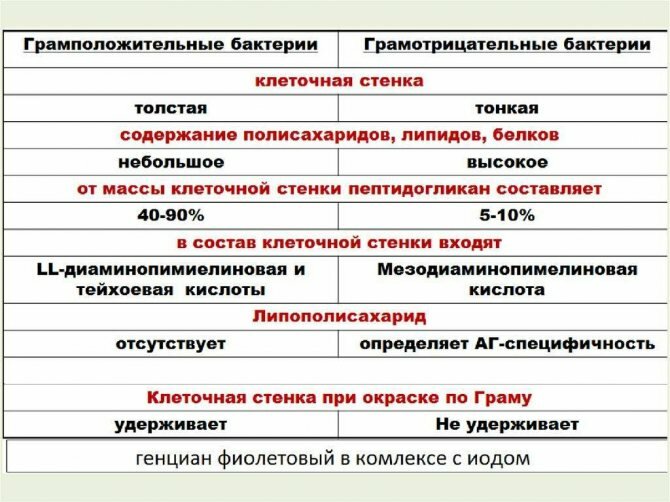
Основная разница — грамположительные и грамотрицательные бактерии
Грамположительные и грамотрицательные бактерии — это два типа бактерий, различающихся по методике окрашивания по Граму. Окрашивание по Граму было разработано Кристианом Грамом в 1884 году. Пятно, используемое во время этой техники, было кристаллическим фиолетовым. Грамположительные бактерии более чувствительны к антибиотикам из-за отсутствия внешней мембраны. Поскольку грамотрицательные бактерии содержат наружную мембрану, они менее восприимчивы к антибиотикам. Следовательно, грамотрицательные бактерии являются более патогенными по сравнению с грамположительными бактериями. главное отличие между грамположительными и грамотрицательными бактериями является то, что грамположительные бактерии содержат толстую пептидогликановую клеточную стенку вместе с тейхоевой кислотой, что позволяет бактериям окрашиваться в пурпурный цвет во время окрашивания грамм, тогда как грамотрицательные бактерии содержат тонкую пептидогликановую клеточную стенку без тейхоевой кислоты, что позволяет клеточной стенке окрашиваться в розовый цвет при встречном окрашивании.
Эта статья исследует,
1. Что такое грамположительные бактерии — Определение, характеристики, структура клеточной стенки, примеры2. Что такое грамотрицательные бактерии? — Определение, характеристики, структура клеточной стенки и оболочки клетки3. В чем разница между грамположительными и грамотрицательными бактериями

Какие бывают
Одноклеточные микроорганизмы не имеют оформленного клеточного ядра, а их генетический материал свободно плавает в цитоплазме. Они различаются по природе клеточных стенок, по форме и по генетическому механизму изменчивости.
Формы
Бактерии существую в формах:
- запятых – например, холерный вибрион;
- сферической (кокки) – стафилококк и стрептококк;
- палочковидной (бациллы) – кишечная палочка и сальмонелла;
- спиралевидной (Spirilla) – Treponema и Borellia;
- жгутиковой – бактерии столбняка.

Грамположительные и грамотрицательные бактерии
Некоторые организмы имеют более сложную форму, например, стебельчатую, квадратную или звездчатую.
По отношению к кислороду
- Аэробные, которым необходим газообразный кислород для завершения собственного энергетического цикла. Эти микроорганизмы не могут расти без доступа кислорода.
- Анаэробные, которым для осуществления функций обмена веществ кислород не нужен, более того, он токсичен для большинства из них.
- Факультативно анаэробные – это микроорганизмы, которым для роста или выработки энергии необязательно присутствие кислорода, они могут использовать его, но могут расти за счет анаэробных организмов, такие бактерии характеризуются высокой степенью адаптации.
- Микроаэрофильные, которые лучше растут в атмосфере с пониженным содержанием кислорода.
Бактериальная клетка окружена 2 защитными оболочками: внешней клеточной стенкой и внутренней клеточной мембраной. Некоторые бактерии, например, микоплазмы, не имеют клеточной стенки.
У других микроорганизмов может быть третий, внешний защитный слой, называемый капсулой. Отростки, похожие на хвосты часто покрывают поверхность бактерий — длинные, называемые жгутиками, или короткие, пили, — они помогают им перемещаться и прикрепляться.
Типы
Грамположительные и грамотрицательные бактерии определяются путем метода окрашивания по Граму. Это распространенный метод, используемый для дифференциации микроорганизмов на основе их различных компонентов клеточной стенки.

| Типы грамположительных бактерий | Свойства |
| Актиномицеты | Несут ответственность за возникновение кариеса и нитчатых респираторных заболеваний. |
| Бациллы | Связаны с пищевым отравлением |
| Clostridium | Имеют различные штаммы, вызывающие пищевое отравление, ботулизм, гангрену и столбняк. |
| Коринебактерии | Основная группа не патогенна для человека, но одна из них является возбудителем дифтерии. |
| Энтерококки | Вызывают дивертикулит, эндокардит, но довольно устойчивы ко многим антибиотикам. |
| Гарднерелла | Они связаны с вагинитами. |
| Лактобациллы | Этот род бактерий способствует формированию микрофлоры влагалища. |
| Листерия | Одна из этого рода бактерий опасна для человека, является патогеном плода, ответственны за менингит новорожденных. |
| Микоплазма | Этот род бактерий не имеет клеточной стенки и вызывает ходячую пневмонию. |
| Микобактерии | Они могут вызывать туберкулез. |
| Стрептококки | Являются возбудителями фарингита, некоторые из н6их влияют на осложнения при беременности. |
Грамположительные бактерии не имеют внешней мембраны в отличие от грамотрицательных. Именно по этой причине последние микроорганизмы более устойчивы к антибиотикам. Если инфекция вызвана грамотрицательными организмами, потребуется сильная доза антибиотиков и строгое соблюдение курса лечения, чтобы полностью избавиться от вредных бактерий.
| Типы грамотрицательных бактерий | Свойства |
| Бортаделла | Представляют собой короткие палочковидные организмы, палочку коклюша. |
| Хламидии | Эта небольшая паразитарная бактерия похожа на вирус и является причиной таких заболеваний, как орнитоз, трахома и неспецифический уретрит. |
| Энтеробактерии | Принадлежит к роду анаэробных не спорообразующих бактерий и может вызывать инфекции мочевыводящих путей, инфекции мягких тканей, септический артрит, инфекцию ЦНС, остеомиелит и многое другое. |
| Helicobacter | Этот тип бактерий имеет палочковидную форму и вызывает язвенную болезнь. |
| Клебсиелла | Палочковидная бактерия вызывает геморрагическую пневмонию. |
| Neisseria | Микробы этого вида колонизируют слизистые оболочки, а их патогенные формы являются возбудителем бактериального менингита. |
| Протей | Эта палочковидная бактерия вызывает инфекции мочевыводящих путей, почек. |
| Псевдомонады | Это род аэробных бактерий, обладающих высокой метаболической активностью. |
При попадании плохих микробов в организм человека, они начинают активно размножаться, выделять токсины, повреждая ткани тела и вызывая недомогание. Вредные бактерии называются патогенными, вызывают заболевания, такие как ангина, стафилококковые инфекции, холера, туберкулез и пищевые отравления.